神経膠腫(グリオーマ)は原発性脳腫瘍のおよそ4分の1を占める代表的な悪性脳腫瘍である。
神経膠腫は悪性度に従って4段階に分けられ、悪性度の高い2つの段階のもの(悪性度 3と4)を悪性神経膠腫と呼ぶ。
神経膠腫の中で最も頻度が高く、また最も悪性度の高いのが膠芽腫(グリオブラストーマ)で、手術をしてから放射線治療と化学療法を行っても平均余命は診断から18カ月、5年生存率は10%程度で、治癒は極めて困難とされ、全く新しい機序による治療手段の開発が待ち望まれていた。
G47Δは、口唇に水疱ができる口唇ヘルペスの原因ウイルスとして知られている単純ヘルペスウイルス1型の3つのウイルス遺伝子を改変したもの。
単純ヘルペスウイルス1型は、がん治療に有利な特長を多く備えている。
1)ヒトのあらゆる種類の細胞に感染できること、
2)細胞を殺す力が比較的強いこと、
3)抗ウイルス薬が存在するため治療を中断できること、
4)患者がウイルスに対する抗体を持っていても治療効果が弱くならないこと
単純ヘルペスウイルス1型のゲノムから、正常細胞での増殖では必要でがん細胞では不要なウイルス遺伝子を取り除くことで、がん細胞だけで増えるウイルスを造ることができる。
がん細胞だけで増えるように工夫された遺伝子組換えウイルスは、がん細胞に感染するとすぐに増殖を開始し、その過程で感染したがん細胞を死滅させる。
増殖したウイルスはさらに周囲に散らばって再びがん細胞に感染し、ウイルス増殖、細胞死、感染を繰り返してがん細胞を次々に破壊していく。
一方、正常細胞に感染した遺伝子組換えウイルスは増殖できないような仕組みを備えているため、正常組織は傷つかない。
既存のがん治療用ウイルスに比べて安全性と治療効果が格段に高くなっている。
また、G47Δの特徴としてがん細胞を破壊する過程で、抗腫瘍免疫を惹起するために、G47Δを投与した部位のみならず、投与していないところにあるがんにも免疫を介して効果が期待でる。
さらに、G47Δは、がんの根治を阻むとされるがん幹細胞をも効率よく破壊することが判っている。
単純ヘルペスウイルス1型を用いたウイルス療法が、悪性脳腫瘍で治療効果を示すことがヒトで確認されて実用化に至ったのは、世界で初めて。
G47Δは脳腫瘍のみならず、あらゆる固形がんに有効であることが動物実験で示されており、今後さらに、可及的速やかに全ての固形がんに適応を広げることを目指している。
2013年からからは、前立腺癌と嗅神経芽細胞腫をそれぞれ対象とした臨床試験を実施した。
2018年からは、悪性胸膜中皮腫の患者の胸腔内にG47Δを投与する臨床試験も開始している。
藤堂教授は、全てのがんに効くと見ており、制度の変更を希望している。(現在は各がんについて臨床試験が必要である。)
2021/6/10 韓国地裁、元徴用工らの集団訴訟で訴え却下
「却下」は訴訟の要件を揃えることができず、本案の審理なく裁判を終わらせること。
5月28日の第1回口頭弁論で、原告・被告双方が求めた審理の延長に地裁が応じず、6月10日の判決期日を指定。さらに原告一人一人への連絡なしに期日を急遽変更し、7日に判決を言い渡した。
元徴用工をめぐっては既に2018年に日本企業に賠償を命じる最高裁判決が確定し、その後も同種訴訟で日本企業敗訴が相次いでいた。
韓国大法院は2018年10月、日本製鉄強制徴用の被害者が出した損害賠償訴訟で被害者の勝訴を確定した。日本製鉄(旧新日鉄住金)に対し、戦時中に日本の工場に動員された4人の韓国の元労働者に1人あたり約1000万円の賠償を命じた。三菱重工業に対する判決も確定している。
大法院判決(11対2の決定)は、戦時中に行われた日本統治下の朝鮮半島から日本本土の工場などへの動員は「日本政府の不法な植民地支配や、侵略戦争の遂行と結びついた日本企業の反人道的な不法行為」と認定していた。
2020/11/3 韓国地裁、朝鮮女子挺身隊訴訟で 三菱重工資産の売却へ手続き
今回の判決は大法院(最高裁)判決を覆し、徴用問題に関連して正反対の2つの判決が当面共存することになった。1965年に日韓が修交し締結した協定および交渉内容に対して相反した意見となる。
今回の裁判官は、3月29日判決の下記の裁判を担当しており、判決はある程度予想できた。
ソウル中央地方法院は3月29日、元従軍慰安婦の女性らが日本政府に損害賠償を求めた訴訟で1月に勝訴した件で、原告が訴訟費用確保のために日本政府の資産差し押さえを求めたのに対し、これを否定する決定を行なった。
確定判決を有効としつつ、外国の資産への強制執行はその国家の主権侵害にあたる可能性を指摘し、韓国内の日本政府の資産を差し押さえた場合、「憲法上の国家安全保障、秩序維持、公共の福祉と相反する結果を招く」と懸念を示した。
2012/4/21 韓国地裁、慰安婦訴訟2件で原告側の訴えを却下
ーーー
原告らは2015年5月、戦時中に日本本土の工場に強制動員されたとして、三菱重工業や日本製鉄、三井造船(現・三井E&S)、ENEOS、住友金属鉱山、三菱マテリアルなど17社を相手取り提訴した。
5月に入り、原告側が1社に対する訴えを取り下げて被告が16社となり、公示送達の効力が発生した後の5月28日に第1回口頭弁論が開かれ、即日結審していた。
日本企業側は、1965年の日韓請求権協定で解決済みとする日本政府の見解に沿って賠償責任はないと主張した。
判決で裁判所は、「原告側の請求権は韓日請求権協定によりすぐに消滅したり放棄されたとはいえない」が、「韓国国民が日本や日本国民を相手にして権利の行使をすることは制限される」とし、「この事件の請求を認めることは、国際法違反の結果を招き得る」と指摘した。
さらに、仮に原告の請求を認める判決が確定し、強制執行に至った場合、「国家の安全保障や秩序維持を侵害するため権利の乱用に該当する」とした。
大法院が日本の植民地支配を「不当」としたことについても「不当性は国際法的に認定されていない」とした。
大法院全員合議体のうち、「個人の請求権は行使できない」とした少数意見(2人)の法理を引き合いに出した。
原告側はすぐに控訴することを決めた。
韓国では、これが大法院に行った場合、控訴審の結果がどのように出てきても、大法院が3年越しに自分たちが下した判決を否定するのが容易ではないため、従来の判例を維持するという見方が支配的である。
付記 原告側は6月14日、裁判所の損害賠償請求訴訟却下判決を不服として控訴した。
韓国内では裁判官への批判が殺到している。
与党代表は判決直後「朝鮮総督府京城裁判所の判決なのか疑われる」という表現まで使って判決を猛非難した。該当判事を弾劾しようという青瓦台の国民請願掲示サイトへの投稿は1日で20万人以上になったという。
バイデン大統領が上院共和党のグループとの間で進めていたインフラ投資計画(American Jobs Plan )を巡る交渉が決裂した。
サキ大統領報道官は、大統領が別の民主、共和両党の上院議員に接触し「超党派の提案をつくるよう求めた」と表明した。
ーーー
バイデン大統領は3月31日、国内のインフラの整備等に8年間で2兆2500億ドルを投入する新たな計画 American Jobs Plan を発表した。
2021/4/2 バイデン大統領、American Jobs Plan 発表、8年間で2兆2500億ドル投資
これに対し共和党は4月22日、対案として、期間5年、総額5,680億ドル計画を発表した。道路や橋などのインフラ事業とブロードバンドに絞ったもの。
ブロードバンドは政府案では1,000億ドルだが、共和党は650億ドルとした。
増税を見込んでおらず、電気自動車の利用料や未使用の連邦資金などで財源を賄うとしている。州や自治体に拠出を要請する可能性もある。
政府・議会間の調整は、議会側は民主党Chris Coons、共和党Shelley Capitoの両上院議員の主導で進められた。
バイデン大統領は5月21日,雇用計画法の歳出規模を当初案2兆2500億ドルから1.7兆ドルに縮小すると発表した。
新提案では、高速ブロードバンド向け投資が1,000億ドルから650億ドルに圧縮される。
道路や橋、主要インフラ向けも当初の1,590億ドルから1,200億ドルに減額される。
R&D、中小企業、サプライチェーン改善などの投資は別の法案に振り替える。
これを受け、米上院共和党は5月27日、9,280億ドル規模のインフラ投資計画の対案を新たに示した。
共和党案は8年間で道路や橋の整備など伝統的なインフラを中心に資金を投じる。政権側がめざす教育分野などへの支出は含まない。
政権側は企業増税で財源を賄うことを提案しているが、共和党は増税に反対し、新型コロナウイルス対策の未使用の財源を充てるなどと主張した。
バイデン大統領は共和党案を規模が小さいとして拒否し、ここで行き詰った。
大統領は6月8日、共和党Shelley Capito上院議員と短時間の電話協議を行った。
大統領はカピト議員の提示額が低すぎるとして、協議を打ち切る方針を固めた。
サキ報道官は声明で「大統領は、カピト上院議員のグループによる最新の提案ではこの国の基本的なニーズが満たされないという見解を伝えた」と述べた。「大統領が自身の計画を1兆ドル以上縮小する用意があったのに対し、共和党グループは新規投資分を1500億ドル上積みするにとどまった」とした。
カピト議員は声明で「真摯に交渉し、バイデン大統領の望む方向に向けて大きく進展していたことから、大統領の決定に失望している」と述べた。「大統領は財源として増税を含む提案をし続けた」とした。
大統領はツイッターへの投稿で「共和党との妥協点を見いだすことに尽力しているが、年収40万ドル以下の層に対する増税は拒否する」とし、富裕層や企業が公平な負担を求める時との認識を改めて示した。
建材用のアスベストで元建設労働者らが健康被害を受けた問題で、国家賠償請求訴訟を起こしていない被害者らを補償する「給付金制度」に関する新法が、6月9日の参院本会議で全会一致で可決、成立した。
自民・公明両党は2021年2月、最高裁で東京、京都、大阪のアスベスト集団訴訟での国の賠償責任が確定したことを受けて、被害者の救済策を検討する合同の対策チームの初会合を開き、関係者へのヒアリングを行うなどしたうえで具体策を取りまとめる方針を確認した。
これを受け、国と原告団、弁護団が、和解内容を盛り込んだ基本合意書に調印。国が最大1300万円の和解金などを支払うことで合意した。裁判外の被害者を救済する給付金制度の創設についても、基本合意書に盛り込まれていた。
2021/5/19
最高裁、建設アスベスト訴訟で 国と企業の責任認める
これを踏まえ、訴訟に加わっていない被害者や遺族にも、給付金を支給するための法律が、可決・成立したもの。
付記
建設現場でアスベストを吸い込み健康被害を受けた人と遺族に、病状などに応じて550万円から1300万円を支給する給付金について、厚生労働省は2022年1月19日から請求を郵送で受け付ける。
国などの責任を認めた2021年5月の最高裁判所の判決を受けて、裁判を起こしていない被害者と遺族に給付金を支給する制度が新たに設けられた。
建設石綿給付金法のポイント:
▽支給対象者は、石綿の吹き付け作業(1972年10月~1975年9月)や、一定の屋内作業(1975年10月~2004年9月)に従事した労働者や一人親方ら
▽石綿によって生じた健康被害の症状に応じて、1人550万~1300万円を支給
▽被害者側の請求に基づき、厚生労働省に設置された審査会が審査を行い、厚労相が認定、支給する
▽独立行政法人・労働者健康安全機構に支払いのための基金を設置
厚労省は支給対象者数を2054年までの約30年間で計3万1000人と推計、支給総額は最大4000億円を見込んでいる。
米上院は6月8日、拡大する中国の影響力に対抗することを目的とした異例の超党派法案 United States Innovation and Competition Act を可決した。
| 共和党 | 民主党 |
民主系 無所属 |
合計 | |
| 賛成 | 19 | 48 | 1 | 68 |
| 反対 | 31 | 1 | 32 | |
| 合計 | 50 | 48 | 2 | 100 |
様々な分野で中国の影響力に対抗することが狙いで、「米国のイノベーションを一段と後押しし、今後数世代にわたって我が国の競争優位性を維持する内容」としている。
米国の技術や科学、研究に合わせて5年間で総額2500億ドルを投資する。
米国の技術や研究の強化に約1900億ドルを充てる。
米議会が1月に成立させた国防権限法に半導体生産を強化する方針を示したことを受け、半導体・通信機器の生産・研究の強化に約540億ドルを支出する。うち20億ドルは、深刻な供給不足に陥っている自動車向け半導体に充てられる。
政府補助金をてこに国産半導体の育成を急ぐ中国をけん制する狙いがある。
付記
バイデン大統領は2021年3月31日、2兆米ドルを超えるインフラ投資計画 American Job Planを発表した。
大統領は、この中から、米国半導体業界の国内生産回帰の実現に向け、500億ドルを割り当てることを明らかにした。(実際には520億ドル)しかし、最終的にこれをAmerican Job Planから外し、このInnovation and Competition Act に含めた。米国の技術や研究の強化に約1900億ドルに含まれる。
この法案は下院との法案すり合わせに時間がかかり、下院での採決は年明けになる。
上院案にはこのほかにも、米政府の端末で中国系動画投稿アプリ「TikTok」のダウンロードを禁止する内容や、中国政府の支援を受ける企業が製造・販売するドローンを購入できないようにする措置が含まれる。
また、米国でサイバー攻撃や米企業からの知的財産窃盗に関与した中国の組織に幅広い制裁を義務付けるとともに、人権侵害に用いられる可能性のある製品について輸出管理の見直しを規定している。
日本など同盟国との連携強化も盛り込んだ。経済安全保障から人権問題まで包括的な対応策を明記している。
同法案の成立には下院の承認も必要になるが、下院には別の対中法案が提出されており、上下両院は一本化も視野に入れて早期成立を目指す。
バイデン大統領は法案を称賛し、「われわれは21世紀を勝ち取るための競争のさなかにある。この法案でスタートの合図が鳴った。後れを取ることは許されない」と述べた。
中国外交部報道官は9日の定例記者会見で以下の通り述べた。
「米上院がこのほど可決したいわゆる『2021年米国イノベーション・競争法案』の中国に関わる内容は事実を歪曲し、中国の発展路線と内外政策を中傷し、『中国の脅威』を誇張し、中国に対する戦略的競争を鼓吹し、台湾地区・香港地区・新疆・西蔵(チベット)関連の問題において中国への重大な内政干渉を犯し、冷戦・ゼロサム思考に満ちており、交流と協力の強化という中米両国各界の一致した願いに逆行するものであり、中国側はこれに断固として反対する」。
韓国紙に興味深い記事が出た。
Samsung Group がGroupの社内食堂の給食業務を100%子会社に全量発注しているのが独禁法上、問題となっており、Group側が自主的な是正策(「同意議決」)を提案したが、公取委はこれを拒否した。財界関係者は「同意議決の棄却は公取委がSamsungの主な役員を検察に告発し、巨額の課徴金を課すなどの制裁を行うという意味だ」と述べた。
Samsung電子、Samsung Display、Samsung電機、Samsung SDIの4社は系列企業のSamsung Welstoryに社内食堂の給食業務を全量発注し、取引条件をSamsung Welstory 側に有利に設定した疑いが持たれている。
Samsung Welstory は第一毛織の子会社であったが、第一毛織がSamusung 物産と統合し、現在はSamusung 物産の子会社。給食と食材事業を行う。海外進出を図っている。
これが問題となったため、Samsungは今年4月、大企業7社と「団体給食発注開放発表式」を行い、「系列企業や一族経営の会社に随意契約で発注していた社内食堂の団体給食に競争入札を導入し、中小企業などに門戸を開く」とした。
公取委によると、Samsungは是正策(「同意議決」)で、Welstoryが独占してきた社内食堂の運営を開放し、中小・中堅企業への発注を優先的に考慮するとした。給食、食材関連の中小企業375社に融資支援(総額1500億ウォン:149億円)、中小給食業者1000社に衛生、安全教育、メニュー開発コンサルティングなどの費用を支援(総額50億ウォン)、社会福祉法人、保育所など450カ所に食品安全改善支援(総額100億ウォン)などを行うことも提案した。
公取委関係者は「Samsungが5月12日に同意議決を申請し、6月2日に公取委全体会議で棄却を決定した」としている。「近く制裁のレベルが決定される」という。
なお「同意議決」の例で、Appleが韓国の移動通信会社に広告費、修理費を転嫁したとして、公取委の調査を受けていたが、本年2月にAppleが修理費の10%割引などに充てる1000億ウォン(99億円)規模の共生基金の創設を提示し、制裁を受けなかった例がある。
一部からは「Appleよりも大規模な共生支援金を提示し、社内食堂の発注も開放することを決めたのに厳しすぎる」との指摘もある。
そもそも、社内食堂業務を子会社にやらせるのが独禁法違反になるのか疑問だが、異様と見えるほどの多額の貢献を行なう解決策を提案したのを公取委が蹴り、罰金を課すというのは理解し難い。
韓国で財閥に対する批判が強まっている中で、Samsung電子の李在鎔副会長が2015年のSamsung
物産と第一毛織の合併にからんで前大統領への贈賄容疑で起訴され、有罪となり収監されている。
公取委がSamsungに対して一般よりも厳しい姿勢を示しているように見える。
2021/6/12 米国の重要部材のサプライチェーンの点検結果と対策
バイデン米大統領は2月24日、重要部材のサプライチェーン(供給網)を見直す大統領令に署名した。半導体や電池など重点4品目で安定した調達体制を整える。有力企業を抱える同盟国や地域と連携して、中国依存からの脱却を目指す。
先ず重要4品目の供給網を100日以内に見直す。リスクを調べ、それへの対応策の提案を求める。
100-Day Supply Chain Review
| 担当 | 品目 |
| 商務長官 | 半導体と先端パッケージング |
| エネルギー省長官 | 電気自動車用を含む高容量電池 |
| 国防長官 (国家防衛備蓄を担当) |
レアアースを含む重要な金属や特定の戦略的物質 |
| 保健福祉長官 | 医薬品及び医薬品有効成分 |
2021/3/1 米、半導体などの供給網見直し
これを受け6月8日に報告書が公表された。
国内の投資不足や競合国の不公正な貿易慣行により、米国の供給網が脆弱になっていると指摘している。
人工知能(AI)など先端技術のカギを握る半導体について「米国の生産シェアは30年間で37%から12%に低下し、輸入品への依存は米国の長期的な競争力を脅かす」と警告。
国内生産・研究開発支援に少なくとも500億ドルを投じるよう議会に要請したほか、日本や韓国など同盟国を巻き込んで世界的な安定供給体制を目指す「国際フォーラム」を開催する方針を示した。
主な勧告や対策案:
<USTRに「攻撃」チーム>
中国に狙いを定め、米国のサプライチェーンを損なっている不公正な通商慣行をやめさせるための新たな「攻撃チーム」を設ける。
チームを率いるのは中国など外国への制裁関税などの権限がある通商代表部(USTR)。
<商務省は通商拡大法232条>
商務省は米通商拡大法232条に基づく調査を検討している。モーターなどの応用品に使われるネオジム磁石の中国からの輸入問題が米安全保障にどう影響するかを調べる。
<供給制約で作業部会>
米国では木材から鉄鋼に至る供給制約の問題が国内のインフレの懸念をかき立てている。これを解決するため、米政権は作業部会を立ち上げる。
重点的に取り上げるのは住宅建設、建築、半導体、運輸、農業、食品など。
<国防生産法で医薬品生産>
バイデン政権は国防生産法を使って、50~100の重要な医薬品を輸入に頼らず、自国で製造できるようにする取り組みを加速する。
朝鮮戦争中に制定された同法は、既に同政権がコロナ対策でワクチンや他の不可欠な医療用品の生産を増強するのに用いている。
<半導体支援>
商務省は半導体メーカーとエンドユーザーの間の情報の流れを円滑化し情報の透明性向上も進める。半導体不足問題の解決も担う。半導体不足は自動車などの製品の生産を阻害している。
<電池政策>
政府の新作業部会が鉱物の採掘許可に関する法律の手直しを検討する。電池に使われる重要な鉱物について、環境面や労働面や持続可能性の「最も高い基準」を順守しつつ、採掘や加工ができる場所を国内で指定することも検討する。
国際開発金融公社は、重要な鉱物プロジェクトへの国際的な投資を拡大する。
エネルギー省は、先端技術の自動車電池のメーカーを支援する融資に170億ドルを振り向ける。
2021/6/14 ジャパン・ティッシュ・エンジニアリング、自家培養口腔粘膜上皮「オキュラル」の製造販売承認取得
帝人子会社のジャパン・ティッシュ・エンジニアリング(J-TEC)は6月11日、世界初の角膜上皮幹細胞疲弊症に対する口腔粘膜上皮細胞を用いた再生医療等製品「オキュラル」の製造販売承認を取得したと発表した。
本品は、大阪大学大学院医学系研究科(脳神経感覚器外科学(眼科学))の西田幸二教授が開発した技術を導入して実用化した国産の製品である。
ジャパン・ティッシュ・エンジニアリングは2020年9月14日、角膜上皮幹細胞疲弊症の治療を目的とした再生医療等製品である自家培養口腔粘膜上皮(開発名:COMET01)の製造販売承認申請を厚生労働省に行ったと発表した。
オキュラルは、2020年に角膜上皮幹細胞疲弊症の治療を目的とした希少疾病用再生医療等製品に指定されている。
医薬品医療機器等法に基づき厚生労働大臣より指定された希少疾病を対象とする再生医療等製品で、当該指定を受けた場合には、試験研究費に対する助成金の交付、優先的な治験相談および優先審査の実施、再審査期間の延長等の優遇措置が受けられる。
希少疾病用再生医療等製品の指定には、当該再生医療等製品の用途に係る対象患者数が本邦において5 万人未満であること、また、代替する適切な治療法が無い、既存の治療法と比較して著しく高い有効性又は安全性が期待されるなどの医療上特に優れた使用価値を有することが必要とされている。
眼科領域では、2020年3月に製造販売承認を取得した自家培養角膜上皮「ネピック」(2020年3月19日承認取得)につづき、国内第2号の再生医療等製品。
iPS細胞からつくった目の角膜の細胞を患者に移植する大阪大の西田幸二教授(眼科)らのチームの「角膜上皮幹細胞疲弊症に対する他家 iPS 細胞由来角膜上皮細胞シー トの first-in-human 臨床研究」の計画が2019年3月5日、厚生労働省の 厚生科学審議会 再生医療等評価部会で、患者への同意の説明文書の内容などに修正を求める条件付きで了承された。
2019/3/8 厚労省、iPS細胞の角膜移植臨床研究計画を了承
ーーー
ジャパン・ティッシュ・エンジニアリングは富士フィルム子会社であった。
1999年2月1日、ニデック、INAX、 富山化学工業は、名古屋大学医学部口腔外科学講座の上田実教授の指導のもとにヒト組織・細胞を用いた移植組織の研究開発を進め、将来の事業化を模索することとし、新しいベンチャー企業としてJ-TECを設立した。
その後、J-TEC株主の富山化学は富士フィルムの完全子会社となった。
2021年初めのジャパン・ティッシュ・エンジニアリングの大株主は富士フィルム(50.13%)、ニデック(10.40%)であった。
2021年に帝人がTOBを行ない、57.72%の応募全てを買い付けた。
2021/2/2 帝人、ジャパン・ティッシュ・エンジニアリングにTOB
小野薬品工業は6月11日、蛋白分解酵素阻害剤「フオイパン®錠」(一般名:カモスタットメシル酸塩)について、無症状から中等症の新型コロナウイルス感染症患者を対象にプラセボを対照とした国内第Ⅲ相試験を行なっていたが、主要評価項目であるSARS-CoV-2が陰性化するまでの期間を達成しなかったため、開発を中止すると発表した。
フオイパンの有効性を示唆する基礎論文の報告およびヒト血中濃度の関係性を踏まえ、健康成人を対象に既承認用量を超えた用量での安全性確認のために第Ⅰ相試験を実施し、その結果を踏まえて無症状から中等症のCOVID-19患者を対象とした第Ⅲ相試験を実施したが、有効性が認められなかった。
無症状から中等症のCOVID-19患者を対象にプラセボを対照とした多施設共同二重盲検無作為化並行群間比較試験で、フオイパン1回600mg(77名)又はプラセボ(76名)を1日4回、それぞれ最大14日間経口投与した。主要評価項目はSARS-CoV-2が陰性化するまでの期間。
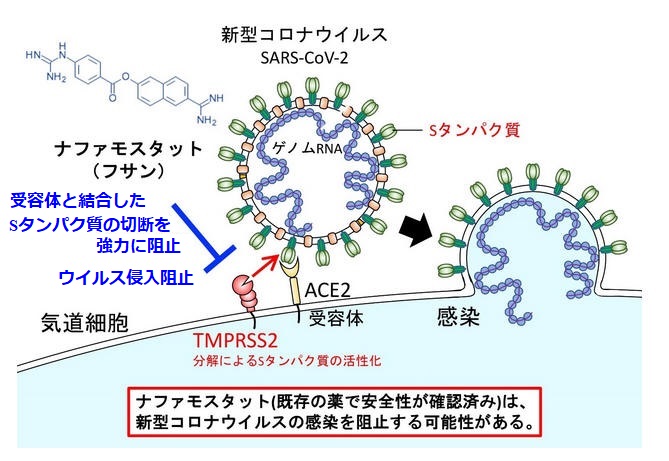
東京大・医科学研究所の井上純一郎教授らは2020年3月18日、急性膵炎の治療薬として国内で長年使われてきた点滴薬剤「ナファモスタット(商品名フサン)」が新型コロナウイルスの感染を阻止する可能性があると発表した。
2020年3月初めにドイツのグループはナファモスタットの類似の薬剤であるカモスタット(商品名フォイパン)の有効性を発表していた。
カモスタット(商品名フォイパン)は、小野薬品工業が創出し、1985年に発売した。既に物質特許は切れており、国内で多数の後発品メーカーが同じ成分の薬を販売している。
2020/3/18 急性膵炎治療薬が新型コロナウイルス感染阻止の可能性
ーーー
なお、フサンについては有望な結果が出ている。
コロナウイルスの場合、ウイルスのSタンパク質がヒト細胞の細胞膜のACE2受容体に結合したあとに、タンパク質分解酵素(TMPRSS2)で切断され、Sタンパク質が活性化されることが重要であるが、ナファモスタット(フサン)はTMPRSS2による切断を阻止し、ウイルスの侵入を阻止する。
2020/5/12 東京大学、アビガンとフサンの併用療法の臨床研究開始
東京大学・井上教授の研究チームの臨床研究では、フサンが変異ウイルスにも効く可能性があると分かった。
実験データでは、フサンの量を増やすとグラフが右下がりになるが、各変異株が同じ動きをしており、変異株にも効く可能性が強いとしている。
但し、医療現場が逼迫するなか、臨床試験が思うように進まないという。井上教授は「年内の承認」を目指している。





.jpg)