2016/7/4
住友化学、ボナックに資本参加
住友化学がボナックの株式を第三者割当増資で引き受け、出資を完了した。
ーーー
2017年9月25日 住友化学 / ボナック
住友化学によるボナックの第三者割当増資の引受(出資拡大)について
住友化学とボナックは、ボナックが第三者割当増資により発行する株式を住友化学が引き受けることに合意し、このたび出資を完了いたしました。これにより、ボナックに対する住友化学の出資比率は19.55%に拡大します。
今回の資本提携の強化を契機に、ボナックが持つ核酸医薬のユニークなプラットフォームと、住友化学グループの医薬品開発、原薬製造、医療診断および安全性分析等の技術をより強固に融合させ、核酸医薬品の早期実用化に向けた開発を加速させます。
ボナックは、次世代医薬品として注目され
ている核酸医薬品を開発しているバイオベンチャーで、日本および欧米の主要国で特許を取得した独自構造のボナック核酸(*1)を用いて、原料開発から創薬探索まで一貫して手掛けています。
住友化学は、2013年にボナックから核酸医薬原薬の製造・販売に関する知的財産権の独占的実施権の許諾を受けて受託製造事業に参入し、2016年には同社へ出資するなど、開発パートナーとして関係を強化し
てきました。
核酸医薬品は、DNA(デオキシリボ核酸)やRNA(リボ核酸)の働きを利用して、病気を引き起こす遺伝子やタンパク質に作用するタイプの医薬品です。副作用を低減した新たな治療薬となる可能性があることから、低分子医薬品(*2)、抗体医薬品(*3)に続く次世代の医薬品として注目を集め、開発が進められています。
実用化に向けては、体内での安定性やDDS(*4)などの課題を解決する必要がありますが、ボナックは、これらの課題解決に有力な独自の核酸医薬のプラットフォームを確立しており、現在は
核酸医薬品開発について国内外の製薬メーカーと共同開発やライセンス交渉を進めているところです。
住友化学とボナックは、今後も核酸医薬品の開発を着実に推し進め、アンメットメディカルニーズの解消をはじめとした医療が抱える課題の解決に取り組んでまいります。
(*1)ボナックが開発した核酸で、従来の核酸が二本鎖構造であるのに対して、一本鎖構造であるのが大きな特徴。その構造により体内での高い安定性と安全性を有する(
(*2)化学合成により作られる一般的な医薬品
(*3)生体がもつ免疫システムの主役である抗体を主成分とした医薬品。標的に対する特異性が高く副作用が少ない点が特徴。大量生産が困難で経口投与できないという課題がある
(*4)Drug Delivery
System(ドラッグデリバリーシステム)の略。必要な薬物を必要な時間、体内の適切な場所に届けることを可能にする技術
2013/11/28
住友化学、核酸医薬原薬の受託製造開始
2013 年11 月22日 住友化学/ボナック
核酸医薬原薬の製造開始について
住友化学と㈱ボナックは、このたび、ボナックが保有する核酸医薬原薬の製造・販売に関する知的財産権の独占的実施権の許諾契約を締結しました。これを受けて、住友化学は、大阪工場(大阪市)に開発用途の核酸医薬原薬の製造設備を新設し、2014
年度第3 四半期から同原薬の受託製造を開始することとしました。
核酸医薬は、DNA(デオキシリボ核酸)やRNA(リボ核酸)の働きを利用して、病気を引き起こす遺伝子やタンパク質に作用するタイプの医薬品です。低分子医薬(*1)、抗体医薬(*2)に続く、第三世代の医薬品として、近年注目されていますが、実用化に至った製品は限られており、本格的な普及に向けては、体内での安定性やDDS(*3)などの課題を解決する必要があります。
ボナックは、これらの課題解決に有力な独自の核酸医薬のプラットフォームを確立し、特許を日本で取得したほか欧米の主要国で出願中です。現在は、国内外の製薬メーカーと核酸医薬品開発についてライセンス交渉を進めるとともに、核酸医薬品の自社開発を行っています。住友化学は、5つの事業部門を有する総合化学企業で、医薬原薬・中間体については、30
年以上にわたる生産実績があり、優れた工業化技術、GMP(*4)対応力を有するとともに、高度な品質保証体制を確立しています。
核酸医薬原薬の工業化パートナーを探していたボナックと、同社の技術の将来性、優位性に着目した住友化学のニーズが合致したことから、今回の決定にいたったものです。
住友化学は、今後、ボナックおよび同社からライセンスを受けて医薬品開発を行う国内外の製薬メーカー向けに核酸医薬原薬の受託製造を行い、医薬化学品事業の強化を図る考えです。ボナックは、住友化学から安定的に高品質の核酸医薬原薬を確保し、核酸医薬品の早期実用化に向けた開発を進めてまいります。
(*1)低分子医薬:化学合成により作られる一般的な医薬品(*2)抗体医薬:生体がもつ免疫システムの主役である抗体を主成分とした医薬品で、標的に対する特異性が高く副作用が少ない点が特徴。大量生産が困難で経口投与ができないという課題がある。
(*3)DDS:Drug Delivery
System(ドラッグデリバリーシステム)の略で、必要な薬物を必要な時間、体内の適切な場所に届けることを可能にする技術。
(*4)GMP:Good Manufacturing Practice
の略で、製造工程における製造管理、品質理の基準を指す。原材料の入荷から製造、最終製品の出荷にいたるすべての過程において、製品が安全に作られ一定の品質が保たれるよう定められている。
・株式会社ボナック
設立 :2010 年2 月
所在地:福岡県久留米市
資本金:950 万円(2013 年10 月31 日現在)
従業員:19 名(2013 年10 月31 日現在)
代表取締役社長:林宏剛
事業内容:核酸合成製造委託事業、核酸系合成技術コンサルティング事業、核酸フォーム関連特許ライセンス事業
ーーーーーーーー
2013/11/16 日経
住友化学、副作用少ない「核酸医薬品」原料生産 VBと連携
住友化学は病気を引き起こす遺伝子に直接働き掛けて治す「核酸医薬品」原料の生産に乗り出す。バイオベンチャー(VB)のボナック(福岡県久留米市)と組み、来秋から生産する。同医薬品は副作用が少ないうえ、薬効が高いと期待されることから製薬各社が注目している。医薬品原料国内最大手の住友化学の参入で普及に弾みがつきそうだ。
核酸医薬品の原料は、日東電工の米子会社と米アジレント・テクノロジーAgilent
Technologiesが合計8割程度の世界シェアを持つ。同医薬品の開発も海外勢が主導している。今回の住友化学の参入で原料の調達ルートが多様化し、日本の製薬会社を巻き込んだ開発競争が加速しそうだ。
住友化学は核酸医薬品を開発するボナックと同社が持つ原料の生産・販売権の利用許諾契約を結んだ。大阪工場(大阪市)に設備を新設し、
2014年秋から主成分の核酸をつくる。投資金額は非公表。同医薬品を開発する国内外の製薬会社から生産を受託する。数年内に年間10億~20億円の売上高を目指す。
遺伝子にじかに働きかける核酸医薬品は、従来型の医薬品と比べて治療効果が高く、副作用が少ないとされる。ただ、病気を起こす遺伝子まで到達することが難しいことから、現状では米ファイザーの目の難病治療薬など3製品しか市販されていない。

ただ、がんや心臓疾患などへの利用も見込まれるほか、従来型の医薬品原料の合成技術を応用できることから参入を決めた。現在、核酸医薬品の市場規模は数十億円にとどまるが、20年には5千億円に広がる見通しだ。
日本ではアンジェスMGと塩野義製薬が共同でアトピー性皮膚炎の治療薬の臨床試験(治験)を実施中。日本新薬は7月、国立精神・神経医療研究センターと共同で筋ジストロフィー治療薬の治験を始めた。
住友化学は原料の需要家でもあるボナックと組むことで、アジレント・テクノロジーなど先行する2社を追う。ボナックなどの開発が進んで市販できる核酸医薬品が出るときは、量産用の設備の建設を検討する。
海外勢の生産能力増強などを受け、エチレンなどの石油化学製品が設備過剰に陥っている。日本の化学メーカーは業績改善に向け、市況や景気に左右されにくい健康・医療分野の事業を強化している。医薬品原料で強みを持つ住友化学は先端医薬品の一つである核酸医薬品原料の生産に乗り出すことで収益基盤を広げる。
http://www.meti.go.jp/meti_lib/report/2011fy/E001922.pdf


。受託製造企業市場はAvecia、Agilent の米国2 社が2 強という構造。市場規模は110 億円前後と推測される。しかし、業界大手
Avecia は日東電工に2011 年に買収された。

林化成
(ボナック)
核酸製造大阪
ST Pharma(韓国)と提携し、核酸医薬品の受託製
造ビジネスを行っている
ーーーーーーーーーーーーーーー
核酸医薬というと、以前から、アンチセンス、アプタマー、siRNA医薬、デコイ、リボザイム、最近では免疫賦活剤(アジュバント)も含め、さまざまなものが提案されてきましたが、現実に日本で承認を取得したのは血管内皮成長因子(VEGF)を抑制するアプタマーである加齢黄斑変性症治療薬の「マクジェンMacugen」(ファイザー)のみ。海外に目を転じても、マクジェン以外では米国でサイトメガロウイルスによる網膜炎を治療するアンチセンス「Vitravene」が98年に承認されているぐらいです。また、マクジェンよりもVEGFに対する抗体断片の「ルセンティス」の方が効果に勝るという判断が下され、少し向かい風が吹く状況にありました。
ーーー
核酸医薬でも、上市されたのは、サイトメガロウイルス性網膜炎治療薬「ヴィトラミューン」(ISIS、アンチセンス)と加齢黄斑変性症治療薬「マキュジェン」(ファイザー、アプタマー)の2品目のみで、いずれも眼性疾患である。+「Kynamro」
第1号は1998年に米国で認可されたエイズ患者のサイトメガロウイルス網膜炎の治療薬「Vitravene」(fomivirsen)です。 Vitraveneは天然型のDNA製剤。こうした第一世代のアンチセンスDNA医薬の問題は、注射すると血中で分解されることと、細胞内になかなか取り込まれないこと。そのためVitraveneは患者の眼球に局所注射して分解を抑止、局所のアンチセンスDNAの濃度を上昇させてやや無理矢理細胞内に取り込ませて薬効を発揮しました。つまり天然型のDNAを使った第一世代のアンチセンス医薬は全身投与できず、対象疾患も極めて限定されたものだったのです。
Vitraveneも開発したIsis社の苦難はここから始まりました
米国食品医薬品局は2013年1月29日に家族性高コレステロール血症の治療薬として、「Kynamro」(mipomersen)を製造・販売認可しました。アポたんぱく質B100のmRNAを標的とした第二世代のアンチセンスDNA医薬です。米Isis
Pharmaceuticals社が開発、米Genzyme社が販売します。循環器系の副作用のため、かなり長い時間、最終認可の判断まで揉めたのですが、家族性高コレステロール血症患者のホモザイゴート(両親からLDL受容体の変異を共に遺伝した患者)に限定して、FDAは認可を与えました。
ーーーーーーーーーーーー
核酸医薬
核酸医薬
DNA(デオキシリボ核酸)やRNA(リボ核酸)の成分である4種類の塩基を組み合わせて化学合成する医薬品。
DNAやRNAの働きを利用して病気を引き起こす遺伝子やタンパク質に直接作用するタイプの医薬品。
治療効果が高くて副作用が少ないとされる。
遺伝子やタンパク質の働きを抑える薬剤候補として『RNA干渉薬』や『RNAアプタマー』が先行している。
最近では、病気によって増減したマイクロRNAを投与し、治療につなげる研究も進んでいる。
デコイ型
「大阪大学医学部第四内科の研究グループは、独自に開発した[デコイ型]と呼ばれる核酸医薬の対象範囲を広げ、動物実験を本格的に実施する。
核酸医薬の治療効果を試すのは虚血による脳梗塞や脳出血後の血管の再狭窄など、細胞内にある『NFkB』などの転写因子が発病に関与している疾患。
デコイ型核酸医薬はNFkBなどに結合してその働きをブロックする。研究グループはすでに[心筋梗塞]や[ガンの転移の抑制]にデコイ型核酸医薬が有望なことを確認済み
モルヒネなみの鎮痛効果
2012年、東京大学発のベンチャー「リボミック」は、ガンなどの痛みに対してモルヒネ並みの鎮痛効果を発揮する新薬候補を開発した。
神経細胞の成長を促す「神経成長因子」(NGF)というタンパク質の働きを抑える物質の生成手法を確立した。
NGFは痛覚系神経の形成に欠かせないタンパク質で、痛みの原因物質とも呼ばれる。リボミックが開発した新薬候補はNGFにだけ結合し、痛覚系の神経形成を抑える効果がある。
傷から産生するNGF → 受容体と結合 → 脳に痛みを伝達する
↑
新薬候補物質
日本で物質特許が成立した。
細胞試験や動物実験で医療用麻薬のモルヒネと同等の鎮痛効果と安全性を示した。
・1回の注射で1週間~2週間l効果が持続する。
(麻薬は毎日投与する必要がある)
・習慣性がない
・使用制限がない。
肺線維症
2012年、東京医科大学、ボナック、三重大学などのチームは、バイオ技術を使って肺の難病「肺線維症」の治療薬を開発した。
動物実験で安全性と効果を確認。
8/16の米科学誌プロスワンに発表。
開発したのは肺線維症の原因となる遺伝子「TGF-β」の働きを抑えるRNA(リボ核酸)を使った核酸医薬品。
人の病気を再現したマウスの肺の細胞に気道から核酸医薬品送ったところ、遺伝子の働きを抑え、線維化しなくなった。
核酸医薬品は薬効を発揮する前に、体内の消化酵素に壊されてしまう問題点があったが、研究チームが独自開発したRNAを使用。
マウス10匹以上で過剰な免疫反応などの副作用もなく、治療効果が見られた。
| 現在、低分子医薬品・抗体医薬品に次ぐ新規医薬品として核酸医薬品に対する期待が高まっています。核酸医薬品は疾患に関連するmRNAや
miRNA、タンパク等を標的とするため作用機序が明確であり、副作用も少ないと期待されています。さらに抗体医薬との違いとして合成が可能であるということがあります。近年では第2世代のアンチセンス医薬やRNAi(RNA干渉)を利用した医薬品(siRNAなど)の開発が活発化しています。2008年にはmiRNAを標的としたアンチセンス医薬、静注製剤によるsiRNAの臨床試験も開始されました。ノンコーディングRNAと呼ばれる領域にはまだ解明されていないことも多く、今後、積極的に研究が進められ、新たな医薬シーズになり得る標的が多く創出されることが期待されます。
核酸医薬はそのままだと体内の消化酵素などによって直ぐに分解されてしまう為、ドラックデリバリー技術(DDS)が非常に重要となります。現在、臨床開発が進められている核酸医薬は患部への直接投与によるものが多いですが、今後は新しいDDS技術の開発によって静脈内投与や経口投与など投与方法の選択肢が増え、核酸医薬品の適用分野が大きく広がることが予想されます。
|

http://www.sarr-llc.com/press/Journal_of_Pharmaceutical_Business20110101.pdf
|
ーーーーーーーー
ボナック BONAC Corporation
Bridge Of Nucleic Acids Chemistry 核酸化学の架け橋
2007年7月にリボ核酸関連研究各社と業務提携し、遺伝子機能解析試薬ビジネスに参入
林化成、遺伝子機能解析試薬ビジネスに参入[2007年7月9日]
林化成(本社・大阪市、林久二社長)はこのほど、日本新薬、アルナイラム・ファーマシューティカルズ(米国)、rnai(東京)のリボ核酸(rna)関連研究各社と業務提携契約を締結、rnaを中心にしたバイオ研究用試薬ビジネスに本格参入する方針を明らかに
...
ST Pharma(韓国)と提携し、
2007年06月18日
研究用試薬RNAの販売開始のお知らせ
日本新薬は、自社が進めている核酸事業の一環として、今般、研究用試薬RNAおよびそのデリバリー試薬(LIC)の販売開始を決定致しました。
販売開始時期は2007年7月を予定。今回販売するRNAは、自社で独自に開発した新規合成法(CEM法)によるもので、RNA合成原料である CEMアミダイトを出発原料に用いています。この新技術により、従来法で合成したRNAと比べ、高純度、かつ長鎖RNAを効率的に合成・提供することが可能となります。日本新薬が、昨年12月のユーロTIDES
注1)と今年5月の米国TIDESに出展した際、このCEM法を紹介し、国内外の多くの企業、大学研究者等からも高い評価を受けています。また、同時に販売提供するLICも、自社で開発したカチオニックリポソームであり、細胞に対する毒性が低く、RNAを効率的に細胞質内にデリバリーすることができます。
販売については、林化成株式会社(大阪市北区、社長:林 久二)
注2)に委託し、販売先は国内外の企業や大学、研究機関等を予定しています。
パラグアイ出身三重大医学部のガバザ・エステバン教授(免疫学)らの研究グループは1日までに、肺線維症の原因となるヒトのタンパク質に対し、人工遺伝子を吸入させる手法が効果を発揮することが、マウスを使った実験で分かったと発表した。
2012/8
弊社が開発したBONAC核酸による特発性肺線維症(IPF)の進行を抑える治療法についての論文が米科学誌「PLoS
ONE」に掲載されましたのでご案内申し上げます。
本研究は国立大学法人三重大学・弊社取締役兼任 ガバザ・エステバン 教授、東京医科大学・弊社取締役兼任 黒田雅彦
教授、国立がん研究センター 落谷孝広 分野長、国立大学法人大阪大学 恵口豊 准教授との共同研究の成果です。
| 株主名 |
林化成株式会社
1919年に「胡粉」の製造を主体に創業して以来、各種原料および加工素材の安定供給を目指すとともに、新素材の開発に注力して参りました。
現在、その事業領域はフィラー製造・輸入・仕入販売、食品原料販売、ライフサイエンス研究用試薬販売、ディーゼル・トラックの粒子状物質低減装置の販売と多岐にわたっています。
タルク、カオリン、炭酸カルシウム、マイカ等の輸入やあらゆる無機粉末を扱う鉱物粉末の専門メーカー |
| 事業内容 |
核酸合成製造委託事業(試薬~原薬)
核酸系合成技術コンサルティング事業
核酸フォーム関連特許ライセンス事業 |
核酸化学
近年、RNA
(リボ核酸)の多岐にわたる機能に注目が集まっており、基礎研究から医薬品開発に至るまでRNAオリゴマーの化学合成の必要性が一段と高くなっています。
DNAの化学合成と比較すると、RNAの化学合成では2’水酸基に対する保護基の導入と除去のステップについて考慮する必要があります。
現在最も汎用されている2’水酸基の保護基としてTBDMS (t-butyldimethylsilyl)
基が挙げられますが、カップリング収率が低く(約97%)、合成効率、スケールアップ、長鎖RNA合成等の点で限界がありました。
その後TOM (triisopropylsilyloxymethyl) 基、ACE (bis(2-acetoxyethoxy)methyl)
基などが開発され、従来法に比べ改良がなされてきましたが依然改良すべき点も残されています。
これらの問題点を解決すべく、ボナックでは新しいアミダイトを開発しました。この新規アミダイトはカップリング収率が極めて高く、これまで非常に困難であった長鎖RNA、例えば100塩基の鎖長を超えるようなRNAも合成可能となりました。アミダイトのコストも低く、高収率、高純度の長鎖RNAが合成できる、実用的なRNA合成法の確立です。
(現在特許出願中です。)
さらに、非ヌクレオシドアナログや機能性核酸の開発にも着手しています。
長鎖RNAを医薬品のシーズとして利用するため、ボナックでは核酸医薬品の開発の根本を担う研究に力を入れています。
ボナック核酸プラットフォーム特許
ボナックは、自社の有する高い有機合成・核酸合成技術に基づいて一本鎖核酸による遺伝子発現制御プラットフォーム技術「nkRNA®」「PnkRNA™」(ボナック核酸)を開発し、2012年4月に国内特許を成立させました。
- nkRNA® : 「遺伝子発現制御のための一本鎖核酸分子」 (特許第4968811号)
- PnkRNA™ : 「含窒素脂環式骨格を有する一本鎖核酸分子」 (特許第4965745号)

siRNA(small interfering RNA)とは21-23塩基対から成る低分子二本鎖RNAである。siRNAはRNA干渉(RNAi)と呼ばれる現象に関与しており、伝令RNA(mRNA)の破壊によって配列特異的に遺伝子の発現を抑制する。この現象はウイルス感染などに対する生体防御機構の一環として進化してきたと考えられている。siRNAは線虫や植物における転写後の遺伝子サイレンシング機構(PTGS)として存在することが報告されていたが[1][2]、その後合成のsiRNAがヒトの細胞においてRNA干渉を引き起こすことが分かり[3]、siRNAを用いたRNA干渉は遺伝子をノックダウンする方法として生物学および医薬分野の基礎研究に応用されていると共に、臨床への応用も期待されている。

ボナック核酸は従来のsiRNA(二本鎖短鎖RNA)とは異なる、ユニークな分子内構造(2次構造)を有する一本鎖長鎖核酸を構造的な特徴とします。
既に日本国内で特許が許諾されているため、特定の欧米企業が専有する既存の核酸干渉に関する基盤特許技術に依存することなく、独自の核酸医薬を開発することが可能となります。

薬物送達システム(DDS:Drug Delivery System)事業
現在、医薬品開発において、薬物の治療効果を最大限に発揮させる薬物送達システム(DDS:Drug Delivery
System)が注目されています。
DDSとは、医薬品の病巣へのターゲティング、生物活性、化学的安定性、代謝活性等を調整して、体内の必要な場所に必要量を適切な時間だけ作用させ、医薬品をより効果的に、かつ確実に使用できるようにするものです。
核酸医薬の分野では、RNAが血中で不安定なため特に化学的安定性が求められています。また遺伝子がターゲットになるため特異性が必須であり、創薬においてDDSの確立は大きな課題となります。
これらの背景から弊社では、最先端のDDS研究を推進されている研究機関と核酸医薬に関わる製剤設計並びに薬物輸送システムに関する共同研究を以下の通り行なっております。
--------------------
わが国でsiRNA医薬開発のエンジンだった日本新薬の矢野さん(矢野 純一:日本新薬・研究開発本部本部長)が退任し、POLYI:Cを開発する企業をスピンアウトしたため、もはや同社の蓄積してきたsiRNAの中核技術は失われてと悲観していました。しかし、ボナックが基本的に日本新薬が開発していた独創的な長鎖の一本鎖RNA分子を基本構造としたRNAi医薬を継承、発展させていました。将来、米Isis
Pharmaceuticals社や米Alnylam社、米Carnegie研究所と特許紛争も考えられますが、長鎖(62塩基)の一本鎖RNA分子はこうした企業や機関の特許に抵触しないか、少なくともライセンス交渉可能であるだけの独創性は備えております。
実際には体内で、一本鎖は対合して両端にループ構造を持った一部二本鎖RNA分子が形成されます。これが体内で分子切断を受け、RISCに取り込まれて、mRNAを分解、遺伝子発現を抑止します。既に、動物実験ですがin
vivoの作用を確認しています。ボナック核酸は現在のところ2種類開発されています。既に述べたものはnkRNAと呼びます。siRNA医薬の最大のネックであるTLRに感知され、自然免疫系を配列非特異的に動かし、インターフェロンを誘導する副作用も、nkRNAは回避できることが最大の特徴です。
同社はnkRNAの両端のループ構造をアミノ酸で置き換えたPnkRNAも開発しました。これは特別にDDSなくても細胞内に効率良く取り込まれる特徴があります。sIRNA医薬開発のもう一つの難関であるDDSの問題もクリアできると主張しています。オリゴ核酸医薬の主要標的臓器である肝臓に静脈注射しても効率良く、取り込まれます。ボナックは安定同位体で両端のアミノ酸を標識する技術も確立、今まで難しかったRNAi医薬の体内動態の計測も可能としました。医薬品開発の基本条件をやっとRNAi医薬も揃えることができるようになったのです。また、2本鎖のsiRNAを合成するよりも、一本鎖であるためボナック核酸を合成するプロセスは単純化できます。ボナックは化学合成技術を徹底的に改良、長鎖のRNAを極めて効率良く合成できるよう、重合反応効率を究極まで追求いたしました。工業的生産にも自信を持っているようです。また、RNAの部分はまったく天然型ですので、誘導体による予想外の副作用のリスクも低いと考えています。
では問題はないのか?欠点と言えば、ボナック核酸が何故、どうやってRISCに取り込まれるのか?分かっていないことです。in
vitroの実験では、通常のsiRNAよりも遺伝子発現抑止効果を発揮するまでに時間がかかります。細胞内でボナック核酸が切断される課程を解明すれば、より有効性の高い第三世代のボナック核酸お開発も夢ではないと思っています。日本も捨てたものではありません。
日東電工 2011/2/4
核酸医薬分野の事業拡大を目指す
米国「アビシアバイオテクロノジー社」を買収
日東電工は、米国統括会社日東アメリカスを通して、今後成長が期待される核酸医薬の分野において事業基盤の強化を目的に、米国マサチューセッツ州にある核酸医薬の製造受託分野でトップのアビシアバイオテクノロジーAvecia
Biotechnology社を買収しました。
買収の狙い
アビシアバイオテクノロジー社は、核酸医薬の製造受託分野でトップシェアを誇り、前臨床段階から商業的製造までのステージにおいて、cGMP*製造能力をベースに、分析方法開発、プロセスバリデーション、安定性試験、品質管理及び薬事面サポートと幅広いサービスを提供しています。今回、当社はアビシアバイオテクノロジー社を買収することにより、揺籃期にある核酸医薬業界において以下のようなシナジー効果を発揮し、更なる事業拡大を図っていきます。
1)核酸医薬分野での優位性のある市場ポジション及び顧客ネットワーク
2)ドラッグデリバリー技術を含む、特許・技術の融合
3)当社のポリマービーズ技術を活用した、核酸合成効率の向上と製造原価削減
4)アビシアバイオテクノロジー社の良好な地理的立地と、更なるサービス提供エリアの拡大
*)cGMP: Current Good Manufacturing
Practice((現行の)医薬品等の製品管理及び品質管理に関する基準の略)。米国食品医薬品局の医薬品等の製造、試験に適用される品質管理システムのこと。
核酸医薬分野における事業展開
核酸医薬は、DNAやRNAの機構成分である核酸からなる医薬品で、遺伝子の発現に直接作用することにより、これまで治療が難しかった病気の治療が可能になると期待されており、抗体医薬に次ぐ医薬品として注目されています。
当社は、既に核酸医薬の分野では日東電工テクニカルコーポレーション(100%子会社、本社:米国カリフォルニア州、社長:松本憲嗣)で核酸医薬合成の技術開発を行なっており、今回の買収で核酸医薬の製造受託事業を手に入れることにより、核酸医薬分野での事業基盤の強化を図って参ります。
アビシアバイオテクノロジー社の概要
1)社名 :アビシアバイオテクノロジー (英文 Avecia Biotechnology Inc.)
2)所在地 :米国マサチューセッツ州、ミルフォード
3)事業内容 :核酸医薬の受託製造においてトップシェアを誇り、世界最大の生産能力を保有する。
また主要な製薬会社、バイオテック会社へのサービス提供の豊富な経験を有する。
ーーーーーー
日刊工業新聞2013年06月25
アンジェスMG、アトピー性皮膚炎治療薬の第1相試験を開始
アンジェスMGは24日、アトピー性皮膚炎を適応対象とする経皮吸収型の核酸医薬品の第1相臨床試験を、塩野義製薬と共同で国内で始めたと発表した。メドレックスから導入した経皮吸収技術を応用することで、核酸医薬のように分子量が大きい医薬品の課題である皮膚への浸透性が、どこまで高まるかを実証する。
この医薬品は免疫反応に関係する遺伝子の発現を調節する転写因子「NF―κ(カッパ)B」の結合部位と同じDNA配列を持つ人工遺伝子(核酸)「NF―κBデコイオリゴ」を有効成分とする。炎症性サイトカインの産生を阻害し、過剰な炎症反応や免疫反応に起因する疾患を治療する効果があるという。NF―κBデコイオリゴの有効性自体は、軟こうタイプの製剤を使って別途行った臨床試験で確認済み。
今回は薬物をイオン液体化したり、イオン液体に薬物を溶解したりして皮膚透過性を高めるメドレックスの技術を応用した製剤の安全性を検証する。
------------
2013年05月09日
国産初のアンチセンス核酸医薬品として
デュシェンヌ型筋ジストロフィー治療剤の臨床試験開始
日本新薬は独立行政法人国立精神・神経医療研究センター(小平市、理事長:樋口輝彦、以下
国立精神・神経医療研究センター)と、2009年から共同研究を進めてきたアンチセンス核酸医薬品であるデュシェンヌ型筋ジストロフィー(DMD)治療剤(開発番号:NS-065/NCNP-01)を用いて、今年7月より、医師主導で早期探索的臨床試験を開始する予定ですのでお知らせいたします。本治療剤はジストロフィン遺伝子のエクソン53スキップを目的に開発され、本スキップに応答する変異形式を有するDMD患者さんを対象としており、強力な薬効と高い安全性が期待されるモルフォリノ化合物で合成されたアンチセンス核酸です。
<開発の背景>
デュシェンヌ型筋ジストロフィー(DMD)は、男児に発症する最も頻度の高い遺伝性筋疾患であり、ジストロフィン遺伝子の変異によるジストロフィン欠損で発症し、筋力低下からやがて死に至る重篤な病気です。「エクソン・スキップ治療」は、アンチセンス核酸と呼ばれる短い合成核酸を用いて、遺伝子の転写産物(mRNA)のうち、タンパク質に翻訳される領域(エクソン)の一部を人為的に取り除き(スキップさせて)、アミノ酸読み取り枠のずれを修正する治療法です。これにより正常なジストロフィンに比べると、タンパク質の一部が短縮するものの、機能を保ったジストロフィンが発現して筋機能の改善が期待できます。この治療でスキップの対象となるエクソンは患者の変異形式に応じて異なり、特にエクソン51スキップは適応となる患者の割合が最多であることから、類薬の治験が開始されています。一方、エクソン53スキップの対象患者はエクソン51に次いで多いとされ、また国内ではエクソン51と同等数との報告もあります。エクソン53スキップを標的とした薬剤の開発は、DMD患者の治療における重要な選択肢として期待されていました。
<開発の内容>
このような背景を踏まえ、日本新薬と国立精神・神経医療研究センターは、エクソン53スキップを誘導する治療薬の開発を目標に、2009年から共同研究に着手し、本年2月には本剤NS-065/NCNP-01の共同開発に関する契約を締結しました。国立精神・神経医療研究センターは神経・筋疾患に関して国際的にも屈指の診療・研究施設としての実績を有し、これまでにもマウス及びイヌなどのDMDモデル動物、並びにDMD患者細胞を用いたエクソン・スキップ治療研究について報告しています。また日本新薬は1980年代から取り組んできた核酸医薬品の研究開発を基盤とした、ゲノム創薬及び核酸合成技術を有しています。共同研究の過程において、日本新薬がエクソン53スキップを誘導する核酸配列を網羅的に合成し、両者で最適化を行った結果、DMD治療剤として最適な配列を見出しました。本剤はこの配列を、強力な薬効と高い安全性が期待されるモルフォリノ化合物で合成したアンチセンス核酸です。これまでに得られた非臨床試験の結果からは、エクソン53スキップに応答する変異形式のDMD患者細胞における有効性が確認されており、病状の進行を抑制する作用を期待することができます。
<今後の展開>
本治療剤の臨床試験は、日本で創製されたアンチセンス核酸医薬品としては国内初であり、またエクソン53スキップを目的としたDMD治療剤の臨床試験としても世界初となります。本試験は国立精神・神経医療研究センターが医師主導として実施する早期探索的臨床試験として、審査当局による計画の承認を待ち、本年7月に開始予定となっています。日本新薬は、今後、国立精神・神経医療研究センターと連携して臨床開発を進めることで、2018年の上市を目指します。また両者は本剤の対象とならない変異ジストロフィン遺伝子を持つ患者さんを対象とする治療薬につきましても、本剤の創製で培った知識と経験を生かして研究開発を進めて行きます。
九大やボナックなど、核酸医薬に関する産学連携ベンチャーを福岡市に設立
http://news.mynavi.jp/news/2012/04/20/100/
RNA干渉法を用いた核酸医薬に関する研究開発を進めてきた九州大学(九大)、東京医科大学、ボナックの3者は日本独自の核酸医薬に関する新しい基盤技術を確立するに至り、それを機に眼科領域に特化した、新しい分子標的核酸医薬の開発と臨床応用を本格的に進めるために、2012年3月19日に、産学連携ベンチャー「アクアセラピューティクス」を福岡市に設立したことを共同で発表した。
「RNA干渉」は、特殊なRNA(2本鎖短鎖RNA、siRNA)を介した、メッセンジャーRNA(タンパク質合成で重要な役割を果たす遺伝子:mRNA)の発現を抑制する現象で、広く生命体に備わる生体反応機構として、2006年度のノーベル生理学医学賞の受賞テーマとなった。
RNA干渉医薬は、この生体機構を利用し人工的に2本鎖RNAを導入することで、任意の遺伝子の発現を抑制し、病気の原因となるタンパク質の産生を妨げることで、さまざまな疾患を治療しようとする手法だ。
RNA干渉医薬を含む核酸医薬は、従来の低分子医薬品や抗体医薬などとはまったく異なる作用機序を有することから、これまで治療が困難とされてきた、がん、遺伝性疾患、そのほかインフルエンザやウイルス感染症などへの適用が期待されている。
また、核酸医薬は抗体医薬とは異なり、標的分子の同定から臨床試験開始までに要する期間が格段に短いことがメリットの1つだ。さらには、医薬品(特に原薬)の製造に要する設備は、抗体医薬に比較して単純で小規模であり、設備投資額も含め、安価に製造することが可能な点もメリットとなっている。
つまり、核酸医薬は、低分子医薬品の容易な製造性を持ちつつ、抗体医薬の有効性と安全性を凌駕する可能性を秘めた、次世代の創薬技術として期待されているというわけだ。
しかし、製品として販売されている核酸医薬は世界で1つのみで、多くは臨床開発の難しさに阻まれている。その主な原因は、主要な技術特許が特定の企業により独占されていることで、特に日本国内での医薬品開発は遅々としており、なかなか進んでいない状況だ。
また核酸分子自体の生体内での安定性や、自然免疫応答の亢進による副作用への懸念、さらには、適切な薬物送達技術がハードルとなり、欧米でも医薬品開発は思うように進んでいない。
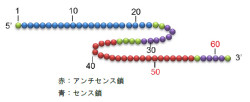
こうした状況の中、ボナックは、日本独自の核酸医薬に関する新規基盤技術として、上記課題を克服することが可能な1本鎖長鎖RNAである「ボナック核酸」(画像1)を開発し、2012年3月に特許査定を取得した(米国・欧州では各国移行審査請求済み)。
|
| 画像1。塩基数が62の場合のボナック核酸(代表例) |
ボナック核酸は、同社が独自に開発した、次世代型の核酸干渉作用を有する基盤技術だ。従来のsiRNAとは異なる、ユニークな分子内構造(2次構造)を有する1本鎖長鎖核酸を構造的な特徴とし、従来のsiRNAが抱える課題であった生体内での安定性が改善されている。
なぜRNAが不安定化というと、体内にはRNAを切断するさまざまな種類の酵素があり、通常、体内に入ったRNAは迅速に分解されてしまうからだ。従って、多くの医薬品候補として用いられているsiRNAは、生体内での安定性を向上すべく、加水分解の起点となる部分を化学修飾することで保護している。しかし、それによる薬理作用の低下、人工的異物としての安全性への問題、さらに製造コストの増大など、新たな課題を生じてしまっているというわけだ。
ボナック核酸は、RNA核酸の3'末端部分が分子内結合により折り返されている、ユニークな分子内構造を有する(画像2~4)。今後より詳細な検討を進めて行く必要はあるというが、ボナック核酸はこうした特徴的な分子内構造により、核酸分解酵素が作用しづらく、生物学的安定性(核酸酵素耐性)の向上に関与しているものと考えられているのである。

|

|
|
画像2。ボナック核酸は分子内に折りたたみ構造(分子内水素結合)を有し、核酸の物理化学的安定性や核酸酵素耐性などが向上している。この形状は「nkRNA」と呼ばれる
|
画像3。nkRNAの折り返し(リンカー)部分を「プロリン誘導体」などのアミノ酸誘導体で置換したボナック核酸の1つの「PnkRNA」
|
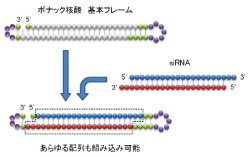
|
| 画像4。ボナック核酸の基本フレームに対して、「カセット化概念」でもってあらゆる配列のsiRNAの組み込みが可能 |
また、ボナック核酸はすでに日本国内にて特許査定が認証されているため、特定の欧米企業が専有する既存の核酸干渉に関する基盤技術(特許)に依存することなく、独自の核酸医薬を開発することが可能という点も大きな特徴だ。
そして、ボナック核酸は従来から使用されている「TBDMSアミダイト」(主要な核酸の合成原料)では効率よく製造することができず、安価に高純度で大量に合成するには高性能なアミダイトが必須となる。
しかし、新たに開発された「EMMアミダイト」は、核酸合成における縮合効率及び製造価格が格段に改善されており、長鎖核酸オリゴマー(比較的分子量が低い重合体)でも安価に高品質で製造することが可能だ。
このように、ボナックは医薬品としての品質・コストに耐え得る原料製造技術、さらには安定同位体核酸を用いた薬物動態法を有する技術の開発にも成功しているのである。
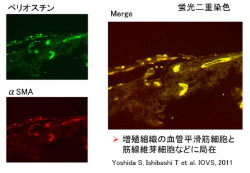
そして、九大大学院医学研究院眼科学分野の石橋達朗教授らは、核酸医薬を用いた画期的な「糖尿病網膜症」治療薬の開発につながる新たな疾患因子として、「ペリオスチンパク質」を独自に同定し、これを新たな標的分子として見出した(画像5)。なお糖尿病網膜症とは糖尿病3大合併症の1つであり、日本では後天性視覚障害原因の約19%を占め、年間約3000人が失明しており、今後も患者数が増加するといわれている。
|
| 画像5。PDR増殖組織でのペリオスチンの局在 |
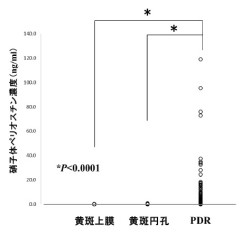
ペリオスチンは、細胞増殖に関与する細胞外マトリクスタンパク質であることが知られている。九大眼科学分野における研究により、ぺリオスチンタンパク質が「増殖糖尿病網膜症(PDR)」(糖尿病網膜症の進行したもの)患者の「硝子体」(眼球の水晶体後方の器官で、ガラス体とも呼ばれる)と「線維血管増殖組織」で対照に比べ有意に上昇していることが初めて見い出され、PDRの進展に関与していることが明らかとなった(画像6・7)。従って、ぺリオスチンは糖尿病網膜症治療の新しい分子標的となる可能性があるというわけだ。
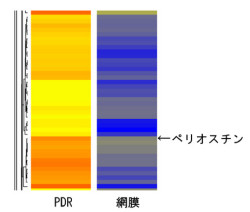
|
|
| 画像6。増殖組織特徴的遺伝子群 |
画像7。硝子体ペリオスチン濃度 |
また、PDRでは網膜上に線維血管増殖組織を生じ、その収縮に伴う「牽引性網膜剥離」が失明の原因となる仕組みだ。現在のところ、線維血管増殖組織生成の機序は十分には明らかになっていない。治療は網膜光凝固術と硝子体手術が行われるが、視機能を十分に保持できない場合も珍しくはないのである。
しかも、現時点で糖尿病網膜症を適応症とし承認されている治療薬はなく、本疾患におけるアンメットメディカルニーズは高く、新薬(新規治療法)の開発が求められているという状況だ。
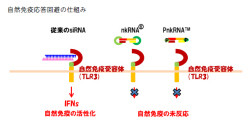
さらに、東京医科大分子病理学講座の黒田雅彦主任教授らは、従来の2本鎖核酸分子に致命的な副作用として問題となっている「自然免疫応答」を、ボナック核酸は回避可能であることを見出し(画像8)、新規な「加齢性黄斑変性症」の治療薬に関する技術を開発したという経緯を持つ。
|
| 画像8。自然免疫応答回避の仕組み |
副作用の問題とは、siRNAを用いた遺伝子の発現抑制には、「Toll様受容体」(動物の細胞表面にある受容体タンパク質で、種々の病原体を感知して自然免疫を作動させる機能を有する)の活性化によるものだ。特にToll様受容体3(TLR3)は、ウイルスの2重鎖RNAを認識することにより活性化され、ウイルスへの防御機能として、インターフェロンなどのサイトカインなどを生成する。
siRNAはこのTLR3を活性化して、サイトカインを誘導する仕組みだ。そしてこの誘導はsiRNAの塩基配列には関係なく、2本鎖という構造に依存することが明らかとなっている。実際、これが理由で米国においてsiRNAによる第III相臨床試験が中断したとの評価があるほどだ。
ボナック核酸は折り返し構造を有するが、そもそも1本鎖であることから、こうした2本鎖RNAによるTLR3活性を回避し、「非特異的炎症誘導」が低減された副作用の少ない新しい治療薬となることが期待されるのである。
そうした経緯を持つ3者が技術を結集し、核酸医薬の開発及び臨床応用に進むべく、この度、アクアセラピューティクスを設立するに至ったというわけだ。
同社には、上記3者が、取締役及び科学諮問委員(SAB)として会社運営に参画し、それぞれに開発してきた特許技術を株式会社アクアセラピューティクスへ技術移転することで、これまで有効な治療薬がなかったさまざまな眼疾患に対し、日本初の核酸医薬品開発を目指す。
まずは、糖尿病網膜症に対する新しい分子標的であるペリオスチン遺伝子をターゲットとする核酸医薬の開発が目標だ。そして2013年10月を目途に前臨床試験、2015年初旬での臨床試験開始を計画している。
2021年10月04日
大分工場に核酸医薬原薬の製造プラントを新設~世界初※1ゲノム編集治療向け高純度のgRNA量産技術を確立~
住友化学は、このたび、世界で初めて※1ゲノム編集治療向けに約90%もの極めて高い純度を有するガイドRNA(gRNA)の量産技術を確立したため、大分工場に核酸医薬原薬の製造プラントを新設することといたしました。新プラント建設により生産能力は現在の約6倍となり、操業開始は2023年半ばを予定しています。
核酸医薬品は、化学合成での生産が可能な低分子医薬品※2と、標的へ作用する選択性に優れる高分子の抗体医薬品※3の特長を併せ持つ中分子医薬品です。DNAやRNAの働きを利用して、病気を引き起こす遺伝子やタンパク質に作用する次世代の医薬品として注目されています。住友化学は、低分子医薬品の原薬および中間体の製造で培った高度な有機合成技術や工業化技術を基に、13年に核酸医薬原薬の受託製造事業を開始し、近年はゲノム編集治療に必要なgRNAと呼ばれる長鎖の核酸医薬原薬の量産化に取り組んできました。
核酸医薬は、DNA(デオキシリボ核酸)やRNA(リボ核酸)の働きを利用して、病気を引き起こす遺伝子やタンパク質に作用するタイプの医薬品で、低分子医薬(化学合成により作られる一般的な医薬品)、抗体医薬に続く、第三世代の医薬品として、近年注目されている。
核酸医薬品は遺伝子にじかに働きかけるため、従来型の医薬品と比べて治療効果が高く、副作用が少ないとされる。
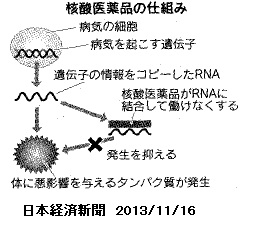
2013/11/28
住友化学、核酸医薬原薬の受託製造開始
ゲノム編集技術は、ヌクレアーゼ(核酸を切断する酵素)を利用して、染色体上の特定の場所にある遺伝子配列を意図的に改変する技術です。2020年10月にノーベル化学賞の受賞対象となったCRISPR-Cas9(クリスパー・キャス9)と呼ばれるゲノム編集技術は、それまでのゲノム編集技術と比較して、編集にかかるコストやスピード、効率に優れるため、現在の医薬品では根治が難しい疾患に対する治療への活用が期待されています。
クリスパー・キャス9を使った治療には、DNA切断酵素としてはさみのような働きをするキャス9に加え、キャス9を標的である遺伝子に導く役割を果たす、高純度で従来の核酸医薬原薬の数倍(約100mer※4)の鎖長を持つgRNAが必要です。
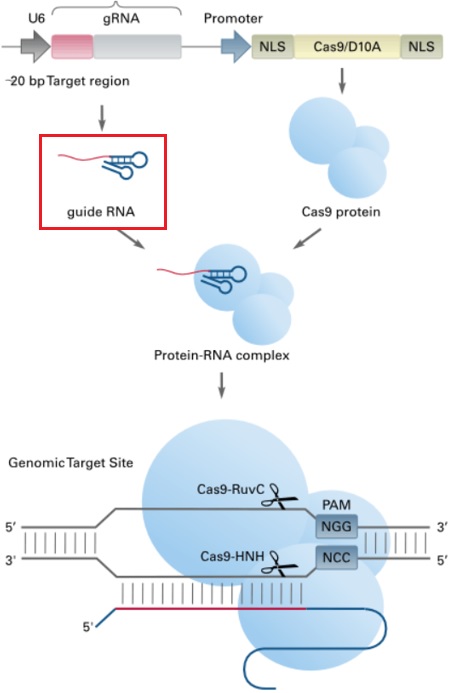
https://www.cosmobio.co.jp/product/detail/crispr-cas.asp?entry_id=14354
住友化学は、これまでの化学合成による製造方法では困難とされてきた、治療用途のクリスパー・キャス9に必要とされるgRNAを約90%の高純度かつ高収率で量産する技術を世界で初めて※1確立したため、製造プラントの新設を決定しました。
住友化学は、19~21年度の中期経営計画において「次世代事業の創出加速」を基本方針の一つに掲げ「環境負荷低減」「ヘルスケア」「食糧」「ICT」の4つの重点分野で新規事業の実現を目指しています。今回の決定を新たな契機に、この先、市場拡大が見込まれるゲノム編集向けgRNA製造のフロントランナーとしての地位の確立を目指すとともに、ゲノム編集治療の普及に貢献してまいります。
※1 gRNAを約90%の高純度で量産する技術について。2021年10月4日発表時点。当社調べ
※2 化学合成により作られる一般的な医薬品
※3 生体がもつ免疫システムの主役である抗体を主成分とした医薬品で、標的に対する特異性が高く副作用が少ない点が特長。大量生産が困難で経口投与ができないという課題がある
※4 merとは、核酸分子の最小構成ユニットであるヌクレオチドが、核酸分子中にいくつ含まれるか、その個数を表す単位
ご参考
住友化学 核酸医薬原薬情報サイト
https://www.sumitomo-chem.co.jp/oligonucleotide/jp/










