ノーベル賞候補・藤田誠氏、創薬に再挑戦 キリンも協力
ノーベル化学賞の有力候補とされる東京大学の藤田誠卓越教授は、未知の分子構造を解析できる「結晶スポンジ法
Crystalline Sponge method」を創薬に使う試みに力を入れる。キリンホールディングスなど10社超の企業と医薬品開発の基盤技術を研究する。
企業と創薬技術などの開発を進める。
分析やソフトウエア開発など:島津製作所、日本電子、(分析装置の)リガク、三井化学分析センター、(分析機器の)ジーエルサイエンス(旧称ガスクロ工業)
化合物提供や活性試験など:日本たばこ産業、ダイセル、キリンHD、高砂香料工業、花王など
三井不動産が設けた三井リンクラボ柏の葉(千葉県柏市)に藤田氏の研究室はある。広々としたガラス張りの部屋に最新の分析装置が並び、ホワイトボードの前で学生らが議論を交わしている。
「明るい研究室の方がたくさんの人が集まる。研究環境にお金をかけることは大事だ」と藤田氏は話す。産学の研究者が集まって知恵を出し合い、新しい創薬手法の確立を目指す。日本医療研究開発機構(AMED)の支援を受けて、5年間で5億円の規模のプロジェクトとなる。
藤田氏は千葉大学助手だった1990年、分子を混ぜるだけで勝手に特定の構造が組み上がる「自己組織化」の論文を発表し、その簡単さで世界を驚かせた。2018年にノーベル賞の登竜門とされるイスラエルのウルフ賞化学部門を受賞した。ノーベル化学賞の有力候補の一人だ。
自己組織化を使って分子の集合体をつくる
私たちの体の中では、生命現象で重要なはたらきを持つタンパク質や核酸などの生体分子が自発的に集まって、機能や構造をもつ“生体組織”となります。これは無秩序な状態から組織立てて秩序を生む現象で、「自己組織化」と呼ばれます。自己組織化は、雪の結晶の成長や、脳内での神経経路の形成など、自然界のいたるところで見られます。
このように、自己組織化は、自然界では頻繁に見られる現象ですが、今から30年ぐらい前までは、自己組織化を利用して人工的にものづくりを行うという発想は化学の世界ではほぼ皆無でした。化学におけるものづくりとは、化学反応によって一つ一つ強固な結合をつくりながら進める事が大前提であり、常識だったからです。ところが東京大学大学院工学系研究科教授の藤田誠さんは、そんな化学の常識を覆し、有機分子と金属イオンを混ぜると今までにない構造の分子の集合体を自己組織化によってつくれることを1990年に発見し、世界に発表しました。以来、自己組織化を使って分子の集合体をつくる研究を続けています。
以下 http://www.spring8.or.jp/ja/news_publications/research_highlights/no_80/
自己組織化の研究が進化し、創薬などに応用できる結晶スポンジ法にたどり着いた。従来、新薬開発のために化合物の構造を調べるには、結晶を作る必要があった。
結晶スポンジ法の登場
学問における大きなブレイクスルーは、えてして全く予想もしない分野から現れます。結晶化という化学100年の難問を解決するアイディアは、一見何の関係もない「超分子化学」というジャンルから現れました。
工学部応用化学科の藤田誠教授は、超分子化学の分野で著名であり、特に自己組織化(単純な化合物同士が自発的に組み上がり、複雑なシステムを形成する)の研究で多くの業績を挙げています。
藤田教授らは、金属イオンとある種の有機化合物が、自己組織化によって3次元的な格子状の結晶を作ることを見出し、長年研究してきました。この結晶は内部に規則正しく空間を残しており、スポンジのような多孔質になっています。
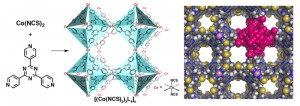
(図1)自己組織化による格子状結晶の形成 藤田研究室
構造を解析したい化合物の溶液に、この「結晶スポンジ」を浸すと、化合物が内部の空間に吸収され、一定の配置に並びます。これをX線結晶解析すれば、目的化合物の構造がきれいに解明できます。運頼みで時間のかかる結晶化というプロセスを経ることなく、極めて微量の試料(最低数十ナノグラム)でも分析が可能です。この結果は2013年に「Nature」誌に掲載され、内外の学会誌などでも「革命的な分析手法」と紹介されるなど、科学界に衝撃をもって迎えられました。

(図2)結晶スポンジ法の概要
© 藤田研究室
結晶スポンジ法は、「不規則な形状の分子が偶然にきれいに並ぶのを待つのではなく、マンションのように仕切られた部屋に入ってもらえばよい」という原理であり、アイディアとしてはごくシンプルです。また、こうしたグリッド状の結晶は「金属有機構造体」(Metal-Organic
Framework; MOF)と呼ばれ、近年世界中で研究競争が繰り広げられている分野です。
にもかかわらず、藤田研究室だけがこの成果に辿り着けたのは、グループの20年にわたる蓄積がものを言った結果です。分子同士の相互作用に関する理解、長年X線結晶解析を行なってきた経験、望みの化合物をデザインして作る有機合成の手法など、これまで積み重ねてきたハイレベルの技術と知識が相まって、初めて得られた成果といえます。
始まったばかりの結晶スポンジ法には、まだまだ改善と発展の余地が残されています。誰もが微量のサンプルの構造を手軽に割り出せるようになれば、文字通りの構造解析革命となります。その日に向け、なお努力は続けられています。
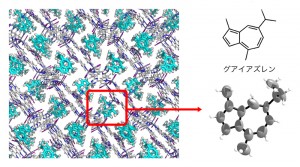
(図3)(図左)結晶スポンジ内の小分子の様子、(図右)結晶スポンジ法で決定されたグアイアズレンの構造
© 藤田研究室
結晶は分子が規則的に並んでおり、放射線の一種X線を当てて、解析すれば立体構造が分かる。ただ、結晶作りは困難で、条件を探すのに数年を要する場合もある。
この課題を解決したのが結晶スポンジ法だ。ジャングルジムのような枠組みの物質を化合物の溶液に浸すと、あたかもスポンジのように溶液がしみ込む。化合物の分子は格子の中に1個ずつ入り、規則正しく並び、結晶のように分析できる。
藤田氏らが13年に英科学誌「ネイチャー」で結晶スポンジ法の原理を発表すると、X線解析の課題解決につながるとして注目が集まった。
2017年に製薬企業や化学メーカー、装置メーカーなどと協力体制を築いた。キリンHDが結晶スポンジ法をノンアルコールビールの開発に役立てるなど成果が出たが、本命の創薬はうまくいかなかった。
当時、共同研究に参加した製薬企業の関係者は「医薬品のように分子量が大きい極性分子への適用が困難だった」と振り返る。藤田氏は「自己組織化は後世に残る名曲となったが、結晶スポンジ法はヒット曲止まりの状態」と現状を評価する。
今回、藤田氏は「結晶スポンジ法のこれまでの制約を取り除ける材料」という秘策で再挑戦する。様々な化合物を吸収できるスポンジを開発しており、論文を執筆中だ。
X線回折装置をてがける協力メーカーのリガクは、結晶スポンジで分子構造を分析しやすくする装置やソフトウエア開発を進める。従来は分析ノウハウを習得する必要があった。リガクの菊池貴氏は「結晶学の知識がない人でも調べられるようにしたい」と意気込む。
医薬品開発の現場で導入しようという試みもある。キリンHD傘下の協和キリンは薬効がありそうな活性物質の探索に使っている。
独自のプラットフォームも開発し、混合試料から狙った化合物を単離し、スポンジに取り込んで構造解析する工程を自動化した。キリンHDの谷口慈将氏は「開発が数カ月程度スピードアップした例もある」と話す。
日本たばこ産業(JT)は原薬の合成過程の中間体や最終製品や、体内に入った後の代謝物の構造解析に利用している。同社生産技術研究所の小野木照二所長は「簡便かつ少量で済み、うまくいけば開発速度の向上につながる」と期待する。


