日本経済新聞 2006/9/29-
イノベーション 日本の底力 バイオ
ゲノム医療 異業種が活力
医療、食品産業などにイノベーション(技術革新)をもたらしてきたバイオテクノロジー。米国が優位に立つが、個別の技術では日本にも世界最先端を走る分野が生まれている。日本のバイオ研究の底力を探る。
「あなたの遺伝子タイプでは12%の確率で副作用が起きる可能性があるが、他のタイプの平均よりは低いです」。リウマチ性疾患では世界最大級の医療拠点として知られる東京女子医科大学の膠原病リウマチ痛風センター。医師はパソコンに表示された検査結果を患者に見せながら、治療薬を選ぶ。
同センターは昨年10月、関節リウマチ患者の遺伝子を調べ、2種類の抗リウマチ薬を使い分ける世界初のオーダーメード医療を始めた。重い肺障害などの副作用を避けるのが狙いだ。
「初診者は1カ月待ちの状態。40-50人の希望者に待ってもらっている」。同センターの鎌谷直之教授は患者の反響に手応えを感じている。これまで240人が治療を受けた。
鎌谷教授らは約1千人分の患者の遺伝子情報と副作用などの関係を統計学を駆使して解析。4つの遺伝的な個人差を調べるだけで最適な使用量や重い副作用、合併症を回避する方法を考案した。海外でも反響を呼び、確認試験が行われた。
ヒトゲノム(人間の全遺伝情報)の完全解読から3年。成果を応用すれば遺伝子レベルで病気治療が将来可能になるといわれてきたが、日本ではすでに現実になった。米国でも昨年、抗がん剤の副作用の遺伝子診断薬が実用化されたが、他の分野は日本が先を行く。しかも日本は医療の現場で使いやすいようにシステムをまとめ上げた。
東京女子医科大のリウマチ治療を支えるのは、東芝やNTTデータの技術。東芝は遺伝子の個人差を簡単に見つけ出すDNA(デオキシリボ核酸)チップなどを開発。NTTデータは遺伝情報から副作用の起こる確率を正確に導き出す手法を使い、投薬量や副作用の可能性を患者に分かりやすく説明できるソフトを開発した。
特別な訓練を受けなくても遺伝情報を解析できるし、医師はパソコンの画面を患者に見せて具体的な治療方針を説明できる。
心筋梗塞や脳梗塞の治療でもオーダーメード治療の大規模臨床研究が8月から始まったが、臨床研究の現場を支えるのが島津製作所の解析装置と凸版印刷の専用チップ。血液一滴で済み、90分間で結果が出る。「ベッドサイド診断」が可能になった。日本大学や日本医科大学など20医療機関が参加。患者の遺伝情報から最適な薬の量を割り出し、副作用の回避を目指す。
2020年には市場規模が5兆3600億円に達するとされるゲノム医療。その実現には「ゲノム研究に加え、ゲノム医療の情報を正確に患者に伝える技術を生み出すメーカーの研究開発力が重要だ」と、癌研究会癌研究所の三木義男・遺伝子診断研究部長は指摘する。バイオ分野に進出する異業種企業の力が加わることが、日本のバイオ研究の総合力につながる。
世界が狙う画像診断技術
「ぜひ特許を買いたい」。今年初め、千葉市の放射線医学総合研究所の一室にドイツの大手製薬会社の特許担当者がやってきた。目当ては同研究所の須原哲也グループリーダーと大正製薬などが開発した化合物だ。アルツハイマー病の早期診断や治療薬の開発に役立つ物質として、世界が注目している。
この化合物は脳細胞の「ミクログリア」とくっつく。活性化したミクログリアはアルツハイマー病の原因たんぱく質(アミロイドベータたんぱく)に集まり、除去する力を持つ可能性がある。
須原リーダーらは、新化合物に放射性物質を付けて目印にし、ネズミの脳に入れてアミロイドベータたんぱくが分布する様子を陽電子放射断層撮影装置(PET)の画像で直接見ることに成功した。
ほかにミクログリアとよくくっつく物質は作られておらず、アルツハイマー病診断手法の実現に欠かせない存在だ。
実は製薬会社の担当者は、須原リーダーらが新化合物の論文を発表した3年以上前から特許交渉を打診した。現在も同社の熱意は衰えない。
放医研の開発した技術のように、体内でたんぱく質などの分子の動きを画像化して見せるのが「分子イメージング技術」。PETなどの画像診断機器を使うが、欠かせないのは標的に目印を付ける技術だ。「日本はこの技術で一目置かれている」(須原リーダー)
PETによるがん検診も、目印の開発に日本人が深く関与した。現在最も使われている標識薬剤はブドウ糖に似た物質に放射性物質を付けたもの。井戸逢雄・福井大学教授が約30年前、米国留学時に合成に成功した。そんな経緯もあり、標識薬剤の開発は日本で盛んになった。
「まさかクラゲの遺伝子でがんの転移を追うとは」。6月に開かれた米国遺伝子治療学会。ベンチャー企業、オンコリスバイオファーマが示した写真に会場の聴衆は驚いた。生きたネズミの体内でがん細胞が緑色に光っていた。
クラゲの発光遺伝子を風邪の原因ウイルスに組み込み、がん細胞にだけ感染させて光らせた。正常な細胞には感染しない。会場にいた米大教授は「将来、がん診断に使えるだろう」と指摘。オンコリスバイオファーマの浦田泰生社長も「手術中にがん転移の確認に使えば、再発を防ぐことができる」と話す。
病気予防には体の細胞やたんぼく質の動きをとらえ、病気の前兆をつかむことが不可欠。目では見えない分子や細胞を"視る"分子イメージング技術は有力な武器だ。
日本はPETの普及率が世界一という。分子イメージング技術を応用できる基盤が整っているともいえる。画像診断技術に詳しい大和総研の浅野信久部長は「画像装置や蛍光技術を診断や治療に使う意識が生まれれば、日本には新たな診断技術をリードする下地がある」と指摘する。
技術融合、内視鏡開発促す
「早く見せてくれ」「ぜひ使ってみたい」。国立成育医療センターの千葉敏雄部長は国際学会で海外出張するたびに、知人の医師から新型内視鏡の実用化の見通しについて聞かれる。11月には学会長に頼まれ、インドで開催されるアジア小児外科学会でも発表する予定だ。
この新型内視鏡は体内の様子が立体的に見えるもので、実用に耐える唯一の装置だ。医療機器メーカーの新興光器製作所が、千葉部長とソニーの協力を受けて開発し、日本では2004年から販売している。
米国の内視鏡手術専門医、米カリフォルニア大学のローレンス・ウェイ教授は数年前から「早く米食品医薬品局(FDA)の承認を」と、米国内での実用化を強く要望しており、現在、米国と中国での承認申請を準備中だ。
内視鏡を使った手術に熟練が必要とされるのは、平面的な画像だと臓器や血管の距離感がつかみにくいのが一因。立体画像なら手術は飛躍的にやりやすくなる。新興光器の内視鏡は先端に2つのレンズがついており、2種類の画像で表示する。偏光レンズの眼鏡をかけると立体的に見える。
立体内視鏡は10年前は世界中で研究が盛んだったが、長く見つめると目が疲れやすい問題があり、製品化が難しかった。目が疲れにくい立体画像を表示する余地はあったが、最適なCCD(電荷結合素子)がなかった。そこでソニーが協力、専用CCDを製作し長時間でも目が疲れない適度な立体感を実現できた。
新興光器などはさらに改良を進めており、胎児用に直径が半分以下の5.4ミリメートルという極細の立体内視鏡の実現にもメドをつけている。
原子力研究の成果を内視鏡に応用したらーー。日本原子力研究開発機構は国際熱核融合実験炉(ITER)の保全のために開発した光ファイバー技術で新型内視鏡を実現するため、ペンタックスなどとこんな研究を進めている。
原研の技術を使うと三重構造の光ファイバーが作れる。一本で「患部を照らす」「見る」「レーザーで患部を焼く」という三役が可能だ。何本も手術器具を体内に入れる必要がないし、患部を狙いやすい。肺の奥など狭い個所の腫瘍にも使えそうだ。
内視鏡に関する日本の技術開発は盛んだ。特許庁の調査によると、03年に出願された世界の内視鏡に関する特許出願件数のうち、日本のものが73%を占めている。
特に消化器用の内視鏡の世界シェアでは、オリンパスを筆頭に日本企業がほとんどを占める。日本は海外に比べて胃がん患者が多く、内視鏡で手術する医師の機器への要求も高度になりがちだ。このため、日本は内視鏡の研究が進んでいるといわれる。医療機器の市場は海外メーカーに押されっぱなしといわれているが、内視鏡の世界は奮闘している。
再生医療支える材料技術
筋肉の細胞でできた特殊なシートを手術で心臓に張り、病気で弱った機能を手助けするーー。こんな新しい臨床研究が、年内にも大阪大学医学部付属病院で始まる。
心臓の筋肉が機能しなくなった患者の太ももから筋肉細胞を採取し、シート状に培養してから心臓表面に張ることで回復を促す。従来は筋肉細胞をそのまま心臓に注射する手法が実施されていたが、阪大の沢芳樹教授は「シートにすれば、移植した細胞の生存率が飛躍的に上がることが期待できる」と解説する。
シート化する技術を開発したのは東京女子医科大学の岡野光夫教授ら。培養皿から細胞を取り出すには、酵素でバラバラに分解する必要がある。岡野教授らは特殊な樹脂を皿に敷き、温度を変えるだけで細胞をシート状のまま、はがせるようにした。研究室には米ハーバード大学やマサチューセッツ工科大学をはじめ、海外から多数の研究者が、細胞シートを見学するために訪問する。
細胞シートはすでに角膜の再生などで臨床応用されているが、今年から来年にかけては歯槽のう漏や肺・食道など、各地の大学病院で新たな臨床研究がスタートする見通しだ。事業化を目指して設立されたセルシードでは、来年6月の欧州での治験開始を目指し、すでに現地の医療機関と交渉を進めている。
「これでようやく海外旅行にも好きなだけ行ける」ーー。東京大学医学部付属病院で6月中旬、五十歳代の女性患者に笑顔が戻った。今春に臨床研究が始まったばかりの新しい骨再生の手術を受けた。患者はがんであごの骨を切除したため、顔の左右が非対称になり、外出にも二の足を踏むようになってしまった。
治療はインクジェットプリンターの技術を応用する。まず、骨の欠けている部分の形状を詳しく測定。この部分にぴったりはまるようにインクジェットプリンターでセラミックス粉末を噴出し、オーダーメードの人工骨を作製する。
セラミックスは人間の体の中で自然分解し、患者自身の骨と置き換わるように設計してある。東大の鄭雄一・助教授らがベンチャーのネクストなどと共同開発した。
骨再生材料は様々な医療機器メーカーが研究し、成果を上げている。米国では死体から採取した骨の移植が主流で、研究自体がほとんどなされておらず、日本の独壇場になっている。米国のような死体骨の移植には死体売買・盗難や感染症の問題もつきまとうため、東大の鄭助教授は「いずれ海外でも日本の骨再生の技術が必要になる日が来る」と期待する。
1970年代に米ハーバード大学で開発された培養皮膚、98年に米ウィスコンシン大学で初めて作製されたヒト胚性幹細胞(ES細胞)ーー。失われた組織や臓器を取り戻す再生医療の研究は、米国で成果が生まれたものが多く、世界をリードしてきた。
だが細部を見れば、技術的に日本が世界の先端を走るケースも出てきた。共通するのは日本が強みを持つ材料技術。モノ作りの経験やノウハウを再生医療に結びつけたことで、世界が注目する分野を築きつつある。
セルシート CellSeed http://www.cellseed.com/
| 再生医療事業 |
●ヒト再生角膜(スティーブンスジョンソン症候群、眼類天庖蒼等対象。角膜ドナーに依存した従来の角膜移植に変わり、いつでも必要なときに再生角膜を医薬品として提供する)
●ペット再生角膜(犬や猫等ペットへの再生角膜提供)
●再生心筋パッチ(虚血性心疾患の損傷部位に貼付し、心機能を劇的に改善する医薬品を提供する。)
●歯周病
●糖尿病性網膜症
●細胞医薬品 |
| 再生医療支援事業 |
●機能性細胞培養器材(細胞シートの培養、脱離及び組織・臓器の構築を可能とする機能性器材を提供する。)
●細胞クローニング用器材
●逆相系分離担体(生体分子の分離精製)
●分取用バイオ医薬品の精製担体
●細胞分離用担体
●細胞・組織を用いた薬効、毒性診断
●毒性薬理試験
●動物試験の代替 |
ネクスト 短時間で再生する人工骨
東京大学医学部の鄭雄一助教授らと医療ベンチャーのネクスト(東京都文京区)などの研究チームは、患者自身の骨に短時間で置きかわる人口骨を開発した。この人工骨は、カルシウムの粒子を1ミリ単位で積み重ね、病気やけがで損傷した骨の欠損部分をCTで撮影し、幹部にぴったり合うよう人工骨を設計する。血管や骨髄が入り込むよう骨の内部に小さなすき間や穴を作ることもでき、人工骨が患者自身の骨に置きかわるのを早める。犬を使った動物実験で、6カ月で人工骨の一部が犬の細胞に置きかわることがわかった。
薬効高める糖鎖 応用カギ
DNA(デオキシリボ核酸)やたんぱく質とともに、生物の機能を支えている生体分子「糖鎖」。その名はあまり知られていないが、うまく利用すれば、薬の効果を高めるのに役立つ。バイオ医薬研究の一大テーマだ。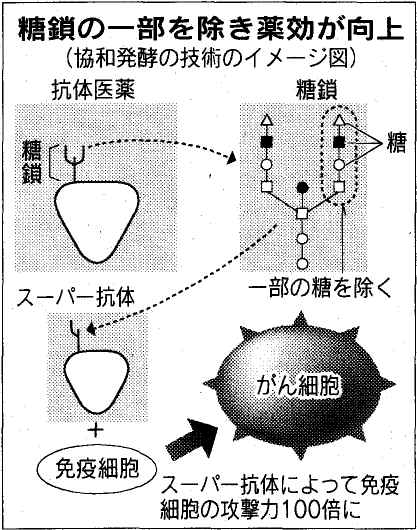
「ライセンス供与先を含め、(糖鎖を利用した)当社の薬効向上技術を使った『抗体医薬』は、世界で約30品目が開発中だ」。協和発酵・医薬戦略企画本部長の立花和義執行役員は、自社技術の影響力を強調する。
抗体医薬は免疫の働きを応用したもので、抗がん剤や関節リウマチ薬など様々な種類がある。日米で約200品目開発されており、協和発酵関連が実に2割弱を占める。
同社の技術では、抗体医薬にある糖鎖の一部を除いた「スーパー抗体」を作ることができる。これを免疫細胞に作用させると、免疫細胞の攻撃力が100倍に強まる。着目する企業は多く、米国の抗体医薬最大手ジェネンテックなど6社に対し技術供与した。
「効果を調べたいのでぜひサンプルを」。北海道大学の西村紳一郎教授のもとには現在も問い合わせが絶えない。
西村教授は2年前に開かれた糖鎖研究最大の国際会議の招待講演で、糖尿痛治療のために塩野義製薬と共同開発した「スーパーインスリン」を発表。インスリンに糖鎖を付けることで、血中にインスリンが長時間とどまり、血糖値を長い時間制御することができたという内容だった。
1日3回の注射が1回で済む可能性があり、患者の肉体的な負担を軽減できると期待される。「2-3年内には臨床試験をスタートしたい」(西村教授)という。
塩野義の創薬研究所長の近藤裕郷執行役員は「インスリンは一つの応用例。他のバイオ医薬品に応用することを検討している」と説明する。北大に共同研究施設を設け、08年にも研究を本格化させる考えだ。
国内の糖鎖研究は長い歴史がある。糖鎖は日本が優位に立つバイオ分野といわれてきた。
例えば、糖鎖を合成する酵素の遺伝子の7割は日本人研究者が突き止めるなど、世界をリードしてきた。協和発酵や北大の研究も、糖鎖研究に注力してきた日本ならではの成果といえる。
だが「成果を応用した糖鎖医薬で日本が優位にあるのはごく一部」と北大の西村教授はクギを刺す。同教授によると、用途まで含めた物質特許は欧米がほとんど押さえている。日本の論文発表は多いものの、応用となると出遅れ感が目立つ。
キリンビールは、貧血治療薬の効果持続時間を糖鎖技術で3倍に高めた次世代製剤を来年にも国内発売するが、その実用化には米アムジェンの技術が欠かせなかった。抗体医薬の効果向上に関しても様々な手法があり、協和発酵の独自技術がどこまで優位性を発揮できるか不透明だ。
北大と日立ハイテクノロジーズが2月に開発した世界初の糖鎖自動合成装置など、糖鎖の工業応用に不可欠な技術は一部で育ってきた。こうした技術を活用し、いかに優れた医薬品を開発できるか。糖鎖の応用研究で日本が主役の座を確保できるかどうか、正念場を迎えている。
▼糖鎖
ブドウ糖など様々な糖が鎖のように連なっている分子で、たんぱく質や脂質と一緒に細胞表面に張り出している。細胞が正常に働くうえで重要な役割を担っている。血液の「ABO型」も、赤血球の表面にある糖鎖の構造の違いから分類されている。糖鎖の複雑な構造やその働きを解明する研究が盛んになっている。 |
| 抗体医薬 |
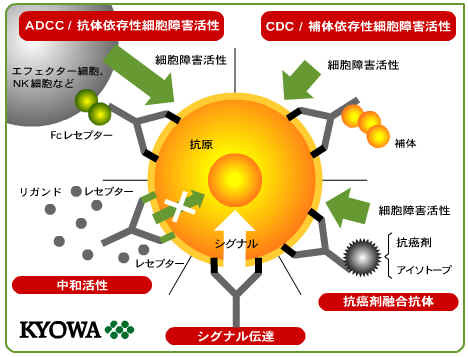 |
ひとの体内には免疫力というすばらしい防御システムがあり、病原菌などの異物が入ってくると抗体がつくられ病気から防いでいます。人体本来のこの働きを活かそうというのが抗体医薬です。抗体が治療効果を発揮するメカニズムには、
- がん細胞が増殖するシグナルを阻害する
- 細胞死シグナルを活性化してがん細胞を殺傷する
- 補体依存性細胞障害活性(CDC)
- 抗体依存性細胞障害活性(ADCC)
などがあります。
|
|
抗がん剤の開発課題に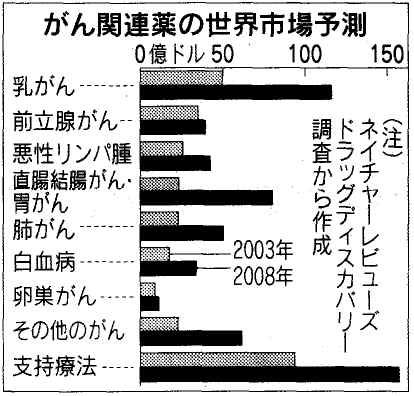
効き目があり副作用も少ない抗がん剤の研究開発。バイオテクノロジー大国を目指す日本にとって、重要なテーマだが、最新治療に使う抗がん剤のほとんどは海外製だ。
中外製薬は4月、「アバスチン(商品名)」と呼ぶ大腸がん向け抗がん剤の承認を申請した。体の免疫反応を利用する抗体医薬というバイオ技術を応用したものだが、開発したのは業界最大手のスイス・ロシュグループの米ジェネンテック。米国で1千億円以上の売り上げ実績を持つ。
「エルロチニブ」「セツキシマブ」「ソラフェニブ」(いずれも一般名)ーー。どれも海外では有名な抗がん剤で欧米の製薬会社が開発した。日本では国の制度の問題もあり承認されていない。
欧米ではロシュはもとより、米ファイザーやブリストル・マイヤーズスクイブなども、抗がん剤に早くから着目していた。理想的な治療薬がなく、患者の満足度が低い分だけ市場を開拓できると判断し、最新のバイオ技術を駆使して開発してきた。がん細胞に現れる特定の分子だけたたく分子標的薬の開発を強化、市場を切り開いてきた。
「(新薬候補を持つ)いいバイオベンチャーがあれば買いたい」。武田薬品工業の長谷川閑史社長はこう公言する。武田は今年、新たに大腸がんや膵臓がんなど6分野に注力する方針を打ち出したが、特効薬と期待される分子標的薬や抗体医薬の開発は、手を着けたばかり。買収も視野にパートナーを探す。二番手のアステラス製薬も「早期に高い開発水準を整えるためには積極的な提携が欠かせない」(田村隼也副社長)と話す。
日本の製薬会社は、生活習慣病治療薬の開発を優先し、抗がん剤分野に注力しなかった。みずほ証券の田中洋シニアアナリストは「がん領域のような(治療薬に対する)満足度の低い市場にいい薬を出せば、高い薬が売れ新市場ができるという戦略が国内製薬会社にはなかった」と指摘する。
がん関連薬は医薬品市場の中でも最も成長率が高い存在になっている。米専門誌ネイチャーレビューズドラッグディスカバリーの予測では、2003年に300億ドル(3兆5千億円)だった世界市場が08年には、593億ドル(7兆円)に倍増するという。
米国で開発中の抗がん剤は約650品目。特にバイオ技術を応用した抗体医薬は160品目と2年前の2倍以上。一方、日本国内での抗体医薬の開発品目は「10分の1にとどまる」(田中洋アナリスト)。フランスのサノフィ・アベンティスに抗がん剤を提供する大鵬薬品工業、がんの増殖を抑える分子標的薬を米国で臨床試験中のエーザイなど気を吐く企業もあるが、ごく一部だ。
欧米の製薬会社は、ジェネンテックをはじめとする有力バイオベンチャーを囲い込み、新たな抗がん剤市場を開拓してきた。日本企業が抗がん剤市場の主役になるには、長期的な戦略で競争力を向上していくことが課題になる。大学や研究機関で生まれた創薬のシーズを育て、抗体医薬などバイオ医薬品の製造技術を磨く努力が欠かせない。
感染症薬、世界レベル遠く
「いざとなったら(海外の)未承認薬を使うしかない」。マラリア治療を手掛ける国立国際医療センター研究所の狩野繁之適正技術開発・移転研究部長はため息をつく。
国内で発生するマラリア患者は年間100人足らずだが、早期治療が遅れれば命を落とすこともある。マラリア治療薬はいくつかあるが、最も有効な薬は欧州で生まれたもので、国内では承認されていない。狩野部長によると、国内約10カ所の病院がこの未承認薬を常備するという。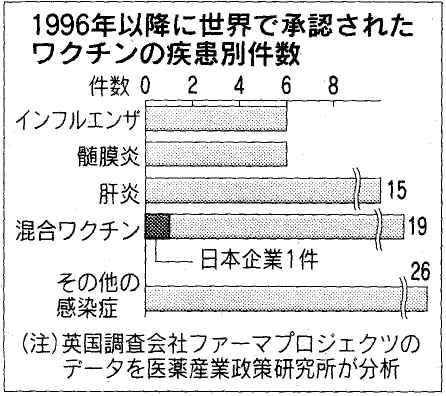
新型インフルエンザ薬も海外頼み。厚生労働省などは世界的大流行に備え、スイス大手製薬メーカー、ロシュが生産するインフルエンザ治療薬「タミフル」を輸入している。予防薬のワクチンも状況は同じ。過去10年間に日本発の新薬はわずか1種類。一方、世界では60種類以上のワクチンが登場した。
日本の製薬企業から、なぜ感染症薬の新薬が生まれてこないのか。狩野部長は「感染症はもうからないため、研究開発に消極的だ」と指摘する。武田薬品工業は1995年に新薬開発の重点領域から感染症を外した。ワクチンメーカーも90年以降、撤退が続いている。
確かに感染症は製薬企業の経営者にとって不確実な要因が多い。糖尿病など生活習慣病に比べて患者数が予測しにくい。新薬を開発して臨床試験する場合、糖尿病などに比べて費用がかさむ。「生活習慣病に比べ薬価が低すぎる」(大手製薬企業幹部)という事情もある。
ただ、海外の製薬企業は感染症の研究開発に力を入れ始めている。英グラクソスミスクラインは、小児などに重い下痢を起こす病気の抗ウイルス薬の開発に注力する。スイスのノバルティスは今年4月にワクチン大手のカイロンを完全買収した。
欧州の製薬企業でも、感染症分野の薬の開発が滞っていた時期があった。しかし新型インフルエンザや重症急性呼吸器症候群(SARS)など感染症への脅威が高まり、将来の巨大市場の可能性を予測して感染症への取り組み強化に動くことになった。
全世界でみれば、死亡原因の約半数は感染症であることも製薬会社を動かしている。
日本で開発できず海外に依存する構図について、感染症に詳しい東京大学医科学研究所の岩本愛吉教授は「国内の安全保障の観点からも問題が大きい」と指摘する。未知の感染症が発生した場合、国内で新薬の開発能力がなければ早期に有効な感染者対策が打てない可能性がある。
日本にまったく望みがないわけではない。富山化学工業は新型インフルエンザの治療薬につながる候補物質を発見した。タミフルを上回る効果が期待されており、米国立衛生研究所(NIH)の協力を得て年明けにも日米で臨床試験を始める計画だ。
熊本大学の満屋裕明教授らの開発したエイズ治療薬は、今夏に米国で承認された。満屋教授は、これまでもエイズ治療薬の研究で世界的な成果を上げている。
いずれも米国の大学との共同研究に発展した。世界と伍していける研究開発力はいくつかある。優れた基礎研究を市場につなぐ研究開発戦略をたて、実行することが問われている。
生まれぬ新薬、治験が壁
「ゲノム(全遺伝情報)が解明されても、新薬につながるプロセスができていない」。日本製薬工業協会が都内で20日開いた記者会見。青木初夫会長(アステラス製薬共同会長)は、日本のバイオテクノロジー研究の現状をこう嘆いた。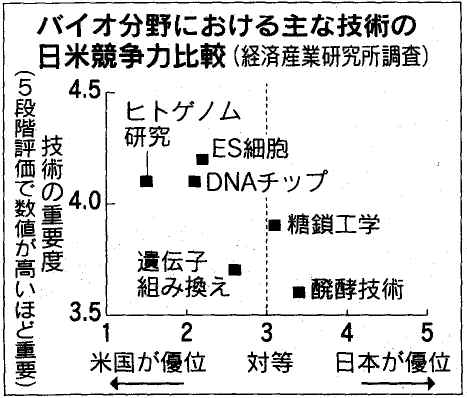
ヒトゲノムの解読が宣言されたのは2000年。病気にかかわる遺伝子の働きが明らかになり、当時、新しい治療薬が続々と登場するといわれた。政府もバイオ関連予算を増やした。しかし当初期待された効果的な新薬は、いまだに患者の手に届かない。
政府の総合科学技術会議の専門委員を務める協和発酵の手柴貞夫技術顧問は「多額の予算投入で(日本の)底力はついてきたが、医薬品の実用化には時間がかかる」と説明する。
確かにバイオ分野の技術力は向上した。経済産業研究所が03年にバイオの主要技術で日米の競争力を比べたところ、ヒト遺伝子の解析や細胞培養などの技術力は00年に比べて上った。全体的にはまだ米国に劣るが、着実に力をつけてきた。
なぜ目に見える成果が生まれないのか。医薬品は安全性などを調べる臨床試験などがあり、新しい物質の発見から薬の実用化まで10年以上。実用化まで平均5年程度といわれるIT(情報技術)や材料に比べて長い。ゲノムも「花開くのは10年以降」(手柴技術顧問)というのが本音だ。
さらに日本の事情として国内の治験期間が米国に比べ1年以上長い。承認審査も含めれば2年を超える。安全性から、期間が短いことがすべていいとはいえないが、日本の承認制度に新薬が生まれにくい最大の原因があるという指摘は多い。
日本は国の承認制度だけでなく、患者への効果を科学的に調べる臨床研究も弱い。
米医学雑誌ニューイングランド・ジャーナル・オブ・メディシンが1991年から10年間に掲載された生命科学分野の国別論文シェアを調べたところ、基礎科学では4位だった日本は臨床研究では14位だった。治験に参加する患者が集まりにくいなどの理由もあるが、医薬品メーカーは「政府は、基礎研究ばかりでなく臨床研究に予算をもっと配分してほしい」と注文する。
バイオ技術が新産業に成長しなければ日本の科学技術全体が衰退する恐れもある。安倍政権は技術革新をテコに経済成長を目指すため、「イノベーション25」を掲げ、医薬品の実用化を「1丁目1番地」として、最も重要な課題に挙げた。
「イノベーシヨンで生まれる画期的な新薬を(社会に)届けるには、医薬品の治験や承認審査の迅速化が課題だ」。柳沢伯夫厚生労働相は10月30日に開かれた医薬品の問題を話し合う厚労省の検討会でこう訴えた。厚労省も安全性を確保しつつ、審査期間の短縮などに取り組み始めた。
世界に通用する新薬を生み出す体制づくりができるかどうか。具体策が問われている。




