キラル
キラルとはギリシャ語の掌に由来することばで、ちようど2種の異性体が右手と左手の関係、すなわち鏡像関係にあることを意味している。
光学異性体
我々が住む世界が三次元であるため生じる異性体。
不斉炭素原子が存在する場合に生じる。
乳酸が余りにも有名。
また、グリシン以外のアミノ酸も光学異性体を持つ。
ある種の物質は、平面偏光をその結晶や液体、溶液に通過させた時、その偏光面が回転するような性質を『光学活性optical astivity』という。
光学活性を示す分子は、分子内に対称面を持たないものである。有機化合物の場合は、炭素原子の結合している相手が全部異なった原子or原子団のものである。このようなタイプの原子は「不斉中心(キラル中心)」と呼ばれる。
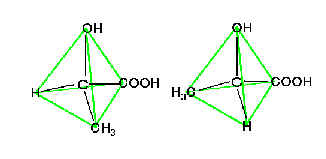
<1>不斉炭素と光学異性体:1.不斉炭素は共有結合で結ばれる4つの原子or原子団がすべて異なるものをいい、分子内に1つの不斉炭素を含むものは互いに鏡像関係の2種の立体異性体を生じる。
2.n個の不斉炭素を持つ分子は2n個の異性体がある。
3.不斉炭素を持ち非対称の分子は、光の偏光面を右or左に回転させる「偏光性光学活性」を持つ。
右旋性を(+)
左旋性を(ー)で表す。<2>光学異性体の分子
化学的にはほとんど同一の挙動を示し、物理的(光学的)性質のみが異なる。このような異性を「鏡像異性」という。
一方の鏡像異性体が偏光面を右に回転すると、他方は同じ大きさだけ左に回転する。
右旋性dextrorotatoryといい、頭文字から「d-」で表記する。
左旋性levorotatoryといい、 「l-]で表記する。<3>d-異性体とl-異性体の等モル混合物:
偏光面を回転しない。つまり光学活性を示さない。
これを「ラミセ混合物」といい、「dl-」で表記する。天然の有機化合物には、光学活性を示すものが多く、しかも多くは一方の対称体のみが得られる。
ex.グルコース:右旋性の異性体しか得られない。
幾何異性体
cis-trans異性体とも言う。
「二重結合は回転出来ない」という性質から生じる。
マレイン酸(cis型)とフマル酸(trans型)の関係が有名。