2005年4月18日
宇部興産
cf ダイセル/キラル
宇部興産、DSM(オランダ)と「キラル技術」で提携
http://www.ube-ind.co.jp/japanese/japanese/news/2005_03.htm
宇部興産(株)(社長:常見和正)は、本日、オランダのDSM
N.V.社(CEO ピーター・エルバディング。以下「DSM」)と、DSMが持つ均一系触媒キラル技術2件(「MonoPhos」と
「Shi Epoxidation Catalyst」。以下「本技術」)
の日本における使用権と技術評価を含む技術導入について、基本合意に達した。
宇部興産が技術導入する意味及び事業展開の可能性
宇部興産は、cGMP対応の設備・ソフトと高いプロセス開発力、そしてカテコール誘導体や複素環合成の技術等をベースに、国内外の製薬メーカーから新薬の製造受託を、開発段階から請負っている。
また、キラル技術の分野では、酵素法による不斉アミノ酸技術を保有しており、この技術を使って国内外の複数の製薬メーカーに新薬中間体を供給している。
宇部興産では、今回、本技術を導入することによって、今まで受託が難しかった不斉水添や不斉エポキシ化工程を含む新薬の製造についても積極的に受託していく意向であり、本技術を必要とする新規案件を、年間数件受託できると期待している。
【用語解説】
(1) キラル技術 :
右手・左手のように、鏡に映った鏡像のような関係にある化合物のどちらか一方(これを光学活性体と言う)を選択的に製造する技術。不斉技術とも言う。
(2) 不斉還元 :
オレフィン等の二重結合に水素を付加することによって、光学活性体を製造する技術。「不斉水添」も同じ意味。
(3) リガンド :
配位子。触媒において、中心の金属の周りに配位している有機化合物。
(4) 光学収率 :
不斉反応において、光学活性体の一方を他方より多く生成する割合。
(5) 2-、3-置換オレフィン : 二重結合に、2個または3個の置換基が付いたオレフィン。
(6) エノールエーテル :
オレフィンの二重結合の炭素にエーテル結合が付いたもの。
(7) 不斉エポキシ化 :
オレフィンの二重結合を酸化しエポキシ基を導入する際、鏡に映った鏡像のような関係にある化合物のどちらか一方を選択的に製造する技術。
(8) エナンチオ選択性 :
鏡に映った鏡像のような関係にある化合物のどちらか一方を選択的に製造する際の選択性。
(9) cGMP対応 : current GMP(Good Manufacturing Practice)。FDA(Food
and Drug Administration:米国食品医薬品局)の要求する医薬品製造基準。
(10) カテコール誘導体 : 2価フェノール誘導体。2価フェノールから派生して製造される化学品。
(11) 複素環合成 :
ヘテロ環合成。酸素・窒素・イオウ等の炭素以外の原子の入った、環状構造を持つ化合物を複素環。ヘテロ環とも言う。
(12) 不斉アミノ酸技術 :
鏡に映った鏡像のような関係にあるアミノ酸化合物のどちらか一方を選択的に製造する技術。
2021 年12 月16 日 宇部興産
ルクサナバイオテク株式会社への第三者割当増資の引き受けによる出資について
宇部興産は、人工修飾核酸化学技術群を基礎としてより安全かつ効率的な新規核酸医薬品の実用化を目指すルクサナバイオテク㈱への第三者割当増資の引き受けによる出資を決定いたしました。
ルクサナバイオテクは、大阪大学大学院薬学研究科・小比賀聡教授の画期的な人工修飾核酸(注)に関する研究成果を社会実装する目的で、2017
年 12 月に設立されました。ルクサナバイオテクは、人工修飾核酸技術のモノマー群(核酸合成物を構成する部品素材)と、これらのモノマー群を核酸合成物に設計する配列デザインノウハウをコア技術としており、これらの技術を基に、核酸医薬品を開発する製薬メーカーとの共同創薬や技術ライセンス提供を実施することにより、未だ薬のない病気に対する治療方法を創出することを主事業としています。
宇部興産は、新規核酸医薬品の創薬ニーズに対するルクサナバイオテクの取り組みに賛同し、出資を決定いたしました。ルクサナバイオテクの創薬力に加えて、宇部興産がこれまで培ってきた低分子医薬品原薬受託製造における高い有機合成・プロセス開発力、生産・品質管理力、承認申請力、および、その供給実績を最大限に活用し、今後需要が高まるとされる核酸医薬品の開発推進に取り組んでいきます。
宇部興産の医薬事業は、技術革新にあふれた「クスリづくり」を地域から発信し、すべての人々の健康に貢献することを目指しています。これからも医療に貢献するため、自社/共同研究開発による「創薬」と「原薬・中間体製造」を両輪として新しい医薬品の種となる化合物を創出してまいります。
(注)人工修飾核酸:天然の核酸(DNA、RNA)に化学修飾を加えることで物性を変化させ、天然の核酸にはない人工的な機能を有した核酸
ルクサナバイオテク Luxna Bioetch 概要
本店所在地
大阪府吹田市山田丘 2 番 8 号
設立日
2017 年 12 月 18 日(事業開始 2018 年 2 月 1 日)
資本金
388 百万円
事業内容
1.
修飾核酸技術の特許サブライセンス事業
2. 製薬会社・バイオベンチャーとの創薬共同研究開発事業
3. アカデミア疾患研究からの自社研究開発事業
4. 核酸医薬品開発支援業務(CMC サポートコンサルテーション)
2005年4月18日 中外製薬
中外製薬、三井物産および実験動物中央研究所と「株式会社
未来創薬研究所」を設立
http://www.chugai-pharm.co.jp/generalPortal/pages/detailTypeHeader.jsp;jsessionid=5THV2YP2DMAM4CSSUIHCFEQ?documentId=doc_5009&lang=ja
中外製薬株式会社[本社:東京都中央区/社長:永山 治](以下、中外製薬)は、革新的な新規医薬品・診断薬のシーズ探索を目的に、三井物産株式会社[本社:東京都千代田区/社長:槍田
松瑩](以下、三井物産)および株式会社実験動物中央研究所[本社:神奈川県川崎市/社長:野村 達次](以下、実中研)との共同出資により、「株式会社
未来創薬研究所」(以下、未来創薬研)を設立することをお知らせします。
なお、営業活動の開始は2005年4月22日を予定しています。
中外製薬と三井物産および実中研は2002年、シンガポールに3社合弁によるPharmaLogicals社を設立し、疾患解析と遺伝子解析など病態およびゲノム情報から効率よく抗体医薬品を生み出す新しいゲノム創薬の研究体制を構築し研究を進めてきました。
それらの成果を薬剤開発に迅速につなげるためには、ゲノム研究の先端的な知見に加え、薬剤分子設計戦略や病態生理学的な研究を融合させた総合的な研究体制構築の必要性が生じてきました。
そのひとつの方法としての未来創薬研は、東京大学先端科学技術研究センター(以下、東大先端研)駒場オープンラボラトリー内に研究拠点を持ち、大学や研究機関が有する先端的な知見や情報に当社の有する薬剤開発技術を融合させることで、革新的な医薬品探索が可能となると考えています。
「株式会社 未来創薬研究所」の概要
1.新会社名 株式会社 未来創薬研究所
(英文表記:Forerunner Pharma
Research Co., Ltd.)
2.本社所在地
東京都目黒区駒場4-2-16
3.資本金 1億円
4.出資比率
中外製薬85%、三井物産14%、実中研1%
5.事業内容
治療薬・診断薬のための新たなターゲットの発見・検証
6.代表者
山崎 達美(中外製薬 取締役専務執行役員)
7.設立日 2005年4月14日
8.営業開始日
2005年4月22日(予定)
9.設立時要員
中外製薬からの出向社員(10名程度)を中心に構成する
2005/04/21 ゾイジーン/富士通
ゾイジーンと富士通が、創薬に関する共同事業を開始
http://www.zoegene.co.jp/releases/050421.pdf
ゾイジーン株式会社(本社:神奈川県横浜市、代表取締役社長:三津家正之、以下、ゾイジーン)と富士通株式会社(本社:東京都港区、代表取締役社長:黒川博昭、以下、富士通)は、2001年より実施してきたバイオIT分野での共同研究の成果を踏まえ、創薬に関する共同事業を開始しました。
本事業は、ゾイジーンの高度な蛋白発現(注1)・結晶解析(注2)・化合物合成などの化学技術と富士通の最新のITを駆使した独自の「de novo SBDD (注3)」創薬手法を中核技術として、新規性および活性の高い化合物の短期間の創出を目指すものです。直近のターゲットとしては、全世界で1,500万人以上の患者がいると推定され、病状の進行を阻止する有効な治療薬が見つからない「アルツハイマー病」の原因酵素と考えられる「BACE-1(beta-secretase)」(注4)の阻害化合物の創出を目指してまいります。
【 共同事業の概要 】
(1)期 間 :今後約1年間とし、その後は両社協議
(2)両社の役割:ゾイジーン:蛋白構造解析、構造設計、合成、試験、マーケティング
富士通 :構造設計、結合予測、マーケティング
(3)事業目標 :2005年度内のヒット化合物の取得、受注
2005年4月22日 JT
JTグループにおける医薬製造拠点の統合について
http://www.jti.co.jp/News/05/NR-20050422/20050422merge_J.html
日本たばこ産業株式会社(本社:東京都港区、社長:本田
勝彦、以下「JT」)とJTグループの鳥居薬品株式会社(本社:東京都中央区、社長:松尾
紀彦、以下「鳥居薬品」)は、JTの医療用医薬品の製造拠点である防府製薬工場と鳥居薬品の佐倉工場を統合することとしました。
これに伴い、防府製薬工場については、2006年3月末をもって廃止する予定です。
JTと鳥居薬品においては、1999年10月以降、グループとしての新薬の研究開発はJTに集中し、また、JTが新たに開発した医療用医薬品については、原則として鳥居薬品が国内での販売を行うという内容の業務提携を行うなど、グループとしての相乗効果を発揮すべく取り組んでまいりました。
日本経済新聞 2005/5/7
新薬「独占期間」延長へ 厚労省8年に 国際競争力高める 後発品参入機会は拡大
厚生労働省は新薬の保護期間を現在の6年から8年に延長する検討に入った。日本の保護期間は欧州に比べ短く、国内の製薬大手などからは画期的な新薬を開発しても投資費用を回収するのが難しいとの声が出ている。欧米の製薬大手による日本への買収攻勢が本格化するとの見方も強まる中で、国内メーカーの国際競争力を高める狙い。一方で保護期間後については後発薬の参入機会を広げて薬の価格の低下を促す。来年の医療制度改革にあわせて実施する方針だ。
キャリア・カフェ・マガジン
05/18/2004
http://www.imca.co.jp/ad/magazine/html/medicalnews_2.html・以前から外資系企業が要望していた、新薬の承認審査のデータ保護期間(製造認可後の有効期間)を欧州と同等の8年とする案に対して、日薬連はようやく重い腰をあげて厚生労働省に要望書を提出しました。政府側で承認されれば、来年度中にも新制度がスタートすることになります。
・もともと新薬の特許期間は20年ですが、これには研究開発期間も含まれるため、新薬承認後の独占的販売期間は実質10年前後というのが通例でした。
そのため、製薬企業は開発期間を短縮し、独占販売期間を長くしようと躍起になっていた訳ですが、これが認められば、正式に『新薬の寿命は8年間』とされるわけで、この8年の間に投資を回収する動きが活発になります。
|
2005/5/11 日本経済新聞夕刊 発表
オムロン、旧日本コーリン買収 米カーライルから100億円強
医療関連を強化
オムロンは医療機器メーカーのコーリンメディカルテクノロジー(旧日本コーリン、愛知県小牧市)を買収する。米投資ファンド大手のカーライル・グループから6月に全株を取得することで合意した。取得金額は今後詰めるが、100億円強となる見通し。カーライルは買収から1年半という短期で、コーリンの再生・売却にこぎつける。
家庭向けの体脂肪計、血圧計などを製造・販売する全額子会社、オムロンヘルスケア(京都市)が株式を取得する。オムロンは医家向け分野に本格進出して医療関連事業を強化し、グループの成長に弾みをつける。
2005/5/11 オムロン
コーリンメディカルテクノロジー株式会社の全株式を取得
http://www.omron.co.jp/ir/ir/press/pdfs/20050511_1.pdf
オムロン株式会社(本社:京都市、代表取締役社長:作田久男、以下オムロン)は、本日(平成17年5月11日)開催の当社取締役会において、当社100%子会社であるオムロンヘルスケア株式会社(本社:京都市、代表取締役社長:赤星慶一郎、以下オムロンヘルスケア)を通じ、コーリンメディカルテクノロジー株式会社(本社:小牧市、代表取締役社長:神部悠三氏、以下CMT)の株式の100%をカーライル・グループ(本社:米国ワシントンD.C.、日本における代表者:安達保氏、以下カーライル)などから取得することを決議いたしましたのでお知らせいたします。なお、本件株式取得は本年6
月中旬を予定しております。
これにより、オムロンヘルスケアは家庭向け血圧計、体組成計をはじめとする家庭用健康医療機器と、CMTのもつ生体情報モニター、血圧監視装置、動脈硬化検査装置などの医療機関向け医療機器を保有することとなり、手術室・病棟から家庭までの幅広いフィールドでの生体計測機器を提供するユニークな企業となります。
2005/5/21 朝日新聞
マツキヨが製薬事業に参入 年内にもメーカー3社買収へ
ドラッグストア最大手のマツモトキヨシは20日、年内にも製薬メーカーを買収することで、製薬事業に参入する方針を明らかにした。買収相手は漢方薬と大衆薬を製造する3社の見込み。同社によると、大手ドラッグストアが薬の製造まで手がけるのは初めて。業界の価格競争が激しくなるなか、製販の一体化で利益の確保を狙う。
日本経済新聞 2005/6/1
「非営利企業」の挑戦 埋もれた薬、安価で販売
シリコンバレーは「バイオバレー」でもある。スタンフォード大のあるパロアルトからサンフランシスコにかけ、バイオ・医薬系新興企業が集積。その中の一つ、サンフランシスコにあるワンワールド・ヘルス研究所は、おそらく世界初の「非営利の製薬企業」だ。2000年の設立で、従業員は40人。ハエが媒介する伝染病で、インドなどで毎年20万人が命を落とす「黒熱病」(内臓リーシュマニア症)への効果が期待されるパロモマイシンを使う治療薬を開発している。
The Institute for
OneWorld Health http://www.oneworldhealth.org/
Fueled by a growing
recognition of global health inequities, Dr. Victoria Hale spent the late 1990s trying to
envision how pharmaceutical science could most impact the lives
of millions suffering from infectious diseases in the developing
world. While a number of international medical organizations were
focused on emergency relief, Dr. Hale knew that the vast majority
of people who were ill still had limited access to safe,
effective, and affordable medicines to treat infectious disease.
New medicines for most tropical infectious diseases did not
exist, and older therapies, if they were available, were often
toxic, difficult to use, or increasingly ineffective due to drug
resistance. As a pharmaceutical scientist, Dr. Hale knew much
more could be done to develop better anti-infective drugs and
vaccines for diseases that disproportionately affect the
developing world and take millions of lives each year.
Supported by a group of dedicated and resourceful pharmaceutical
peers, Dr. Hale led a worldwide effort to uncover potential new
medicines for diseases of poverty and pursue their research and
development. A bold experiment was taking shape -- the creation
of a pharmaceutical company whose decisions could be based on global need
rather than financial opportunity. In response to this unique
approach to improving the treatment of infectious diseases around
the world, doors opened within the biopharmaceutical industry,
within universities, and within the tropical disease research
laboratories of the United States government.
In July of 2000, Dr. Hale founded the Institute for
OneWorld Health,
the first nonprofit pharmaceutical company in the United States.
Its mission was to develop safe, effective, and affordable new
medicines for those most in need.
Drawing upon gifted scientific minds and the innovative business
model they had created, Dr. Hale and her colleagues set out to
develop the pipeline of potential drug leads into approved new
medicines at a fraction of the cost of conventional
pharmaceutical development. To ensure success, the team stressed
partnership and collaboration with industry and international
research institutions. To ensure affordability, they sought
donated and royalty-free licensing of intellectual property and
identified research and manufacturing capacity in the developing
world.
With early investment from the Bill &
Melinda Gates Foundation, collaboration with the World Health
Organization and the US National Institutes of Health, and alliances with biotechnology
firms such as Celera Genomics, OneWorld Health has completed
final stage testing of a promising new therapy to cure visceral
leishmaniasis
in India, and will apply for drug approval in India in 2005.
New therapies for malaria are underway, and diarrhea and
Chagas drug
leads stand ready to be developed. OneWorld Health continues to
vigorously pursue new sources to continue funding development. An
extraordinary journey is well underway.
(株)医学生物学研究所 http://www.mbl.co.jp/index.html
オンコセラピー・サイエンス/医学生物学研究所
癌を対象にした抗体医薬の創薬で提携
→合弁会社
ディナベックと中国に合弁会社
2005/06/16 (株)医学生物学研究所
(株)医学生物学研究所(MBL)とバイオベンチャーのディナベック(株)は、中国(北京)に合弁会社を設立した。
http://www.mbl.co.jp/company/presspdf/press050616.pdf
研究用試薬、臨床診断薬、抗体事業の国内バイオ大手「(株)医学生物学研究所」(西田克彦社長、本社:名古屋市、以下「MBL」という。)と新興バイオベンチャー「ディナベック(株)」(長谷川護社長、本社:つくば市、以下「ディナベック」という。)は北京市内に合弁会社「北京博迩邁生物技術有限公司(英語名 Beijing
B&M Biotech Co., Ltd)」を設立しました。中国の著名な研究者、経営販売経験者も出資しています。新会社は、MBLの研究用試薬、臨床診断薬を中国において一手に販売するほか、抗体、検査試薬の開発、製造も行う計画です。
中国ではこの4月に一連の対日抗議行動が行われ合弁企業設立への影響も懸念されましたが、中国の著名な研究者、経営者との強い信頼関係から予定通りの設立となりました。
新会社の設立にあたって、MBLとディナベックは、すでに中国最大手の製薬会社との間で重症虚血肢の遺伝子治療製剤を導出し癌遺伝子治療等で共同開発を進めているディナベックの持つ中国における事業力とネットワークを活かし、中国現地のバイオ業界の有力者とともに合弁会社を設立することで、中国における事業推進に迅速かつ的確な対応が可能な企業形態としました。
新会社は、中国の先端科学技術推進拠点である北京市中関村にある北京大学の新設インキュベーションセンター内に本社を置き、研究用試薬、臨床診断薬の開発・製造・販売に先行して、北京市サイエンスパーク内のベンチャーの施設・設備を利用した抗体の開発、製造を行います。すでにSPFウサギの供給源を確保し、6月から業務を開始いたします。また、新会社は1年以内に北京と上海に、2年以内に中国沿岸地域での試薬、臨床診断薬の販路を確立し、中国での本格的販売展開をいたします。
この新会社では、2008年に売上1500万人民元、利益300万人民元を目標にしています(2005年5月現在の為替レートで、それぞれ約1億9500万円、3900万円)。
【新会社の概要】
(1) 会社の名称:
北京博尓邁生物技術有限公司(Beijing Boermai
Shengwujishu Yoouxiangongsi)
英語標記: Beijing B&M Biotech Co., Ltd
(2) 主な事業の内容: 医学、生物学および研究用抗原、抗体、薬剤、機器器具の研究、開発、生産及び販売
(3) 設立: 2005年5月
(4) 本社所在地: 北京市海淀区中関村北大街151号資源大厦803室
(5) 役員: 董事長: 朱亜峰(ディナベック)
副董事長: 西田克彦(MBL)
総経理: 駱燮龍(北京医薬集団)
※役員構成:MBL3、ディナベック2、中国側1
(6) 資本金: 400万人民元(2005年5月現在の為替レートで約5200万円)
(7) 株主構成: MBL 67.5%、ディナベック20%、その他12.5%
※新会社はMBLの連結子会社になります。
【株式会社医学生物学研究所の概要】
(1) 主な事業の内容: 臨床検査薬、基礎研究試薬の研究・開発、製造、販売
(2) 設立: 1969年8月
(3) 本社所在地: 〒460-0002 名古屋市中区丸の内三丁目5番10号住友商事丸の内ビル5階
(4) 代表者: 代表取締役社長西田克彦
(5) 資本金: 2,228百万円
(6) 従業員数: 246人(2005年3月末(連結))
(7) 売上高: 4,932百万円(2005年3月期(連結))
【ディナベック株式会社の概要】
(1) 主な事業の内容: 自社ベクター技術に基づく遺伝子治療製剤開発、遺伝子ワクチン開発、
組換えタンパク質の製造、遺伝子・タンパク質の機能解析、プラットフォーム技術としてのベクター技術の開発
(2) 設立: 2003年9月
(3) 本社所在地: 〒305-0856 茨城県つくば市観音台一丁目25番11号
(4) 代表者: 代表取締役社長長谷川護
(5) 資本金: 1,079百万円
(6) 従業員数: 32名(2005年3月末)
2005/7/12 日本経済新聞
日本生薬を吸収合併 ツムラ
11日、100%子会社の日本生薬を10月1日付で吸収合併すると発表した。中国で加工できる体制が整ったため、86人の社員と設備を本体に吸収する。日本生薬の2005年3月期売上局は62億円。
発表
合併の目的
当社は、2006年(平成18年)3月期を初年度とする3カ年経営計画の重要テーマとして、グループ経営の効率化に取り組んでおりますが、今般その一環として、当社の100%子会社である日本生薬株式会社を吸収合併することを決定いたしました。
この合併は、当社グループ内で培った医薬品原料(生薬)の加工・管理・品質保証体制を効率化・強化することを目的としたものです。
日本生薬株式会社は、株式会社ツムラの100%子会社で、生薬を扱う専門企業です。
生薬とは医薬品(漢方薬等)をはじめ、食品等にも利用されている天然植物等を加工(主に乾燥)したものの総称です。
生薬の精製加工には高度な専門知識と特殊な技術が必要とされます。当社は、医療用漢方製剤の製造で培われたノウハウを駆使して、医薬品用生薬の他、食品用の素材、ハーブ、香辛料、野菜等、峻別された良質な原料素材を提供しています。
また、生薬・ハーブなどを利用した商品開発も手がけ、栄養補助食品、園芸・農業資材など自然派の人にやさしい、環境にやさしい製品作りを展開しています。
2005/07/13 オカモト
株式交換によるイチジク製薬株式会社の完全子会社化に関するお知らせ
http://release.nikkei.co.jp/detail.cfm?relID=105318&lindID=4
平成17年7月13日開催のオカモト株式会社(以下、「オカモト」という。)取締役会において、オカモトは平成17年10月1日を期して株式交換によりイチジク製薬株式会社(以下、「イチジク製薬」という。)を完全子会社化することを決議し、株式交換契約を締結いたしましたので、下記のとおりお知らせいたします。本株式交換については、商法第358条(簡易株式交換)の規定に従い、オカモトにおいては株主総会での承認を受けることは予定しておりません。
1.株式交換による完全子会社化の目的
イチジク製薬は大正14年(1925年)に創業以来、浣腸製造販売を主力事業としている会社で、平成17年3月3日においてオカモトの子会社となりました。
オカモトは、「創意あふれる技術を集結して、健康的で快適な人間生活に寄与する商品をつくり出し、当社に関係するすべての人々により大きな満足を与えることをめざす」の企業使命のもと、ゴム・プラスチックなどの化成品メーカーの分野で順調に業績を伸ばしており、今後も独自の技術を基盤に人々の生活に役立つ商品を多面的、積極的に開発し提供していくことを経営方針としております。
このたび、イチジク製薬を株式交換の方法によりオカモトの完全子会社とすることで、株主構成を簡素化しより迅速かつ機動的な意思決定をはかるとともに、取扱商品の拡充、商品の開発・企画力の強化、及び事業体制の共用化等の相乗効果によるオカモトグループ全体の一層の企業価値増大を図ってまいります。
2005年7月19日 株式会社そーせい そーせい
英国のアラキス社の株式取得(子会社化)のお知らせ
http://www.sosei.com/jp/press/pdf/050719-j_press.pdf
当社は、英国エセックスに本拠を置くバイオ医薬品開発企業であるアラキス社の株式を100%取得し、完全子会社とすることを企図して、本件株式取得を実施することといたしました。両社のバイオ医薬品開発事業を統合し、開発パイプラインの拡充および国際的な研究開発体制の強化を図ります。
株式取得の主な流れ
(1) 第三者割当増資
当社は、アラキス社の全株主に対して申し出を行い、申し出に応じた株主に対して1株522,600
円にて計35,630 株の新株式を割り当てるとともに、調整金総額989,091
円を支払い、その対価としてアラキス社の全株主は同社の株式計894,640
株(発行済株式数の88.91%)を現物出資します。
(2) 株式買取
当社は、アラキス社の全株主に対して申し出を行い、申し出に応じた株主から、最大で計111,563
株(発行済株式数の11.09%)を、最大で計2,306,448,909
円の対価にて買い取る予定です。
(3) アラキス社の子会社化
当社は、上述(1)(2)の取引を通じて、アラキス社の全株主が当社の申し出に応じた場合、同社の全株式を取得し、同社を完全子会社といたします。当該株式取得はアラキス社株式の100%取得を目指すものですが、申し出に応じた株式数が一定数に満たない場合には当社は本件取引を中止することがあります。
【株式取得スキーム図】
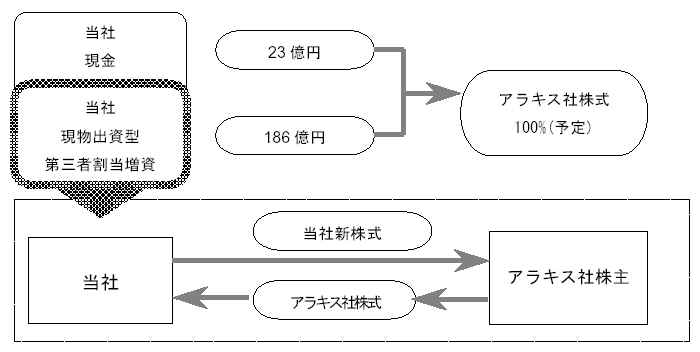
3.異動する子会社の概要
(1) 商号 アラキス・リミテッド(Arakis Limited)
(2) 事業内容 バイオ医薬品開発
(3) 設立年月日 2000 年3月
(4) 本店所在地 Chesterford Research Park, Saffron Walden,
Essex CB10 1XL, UK
(5) 代表者 ケネス・カニンガム(Kenneth Cunningham)
(6) 資本金 138 百万円
(7) 発行済株式総数 1,006,203 株
(8) 総資産 3,552 百万円
(9) 決算期 12月
(10) 従業員数 39名(2005 年7月現在)
(11) 主な事業所 英国エセックス
株式会社そーせい
http://www.sosei.com/jp/
そーせいは医薬品開発に注力する日本のバイオ医薬品会社で、元ジェネンテック株式会社社長の田村眞一氏により1990
年に設立されました。欧米及び日本の企業からの後期開発段階の化合物や医薬品のインライセンス、独自のDRP(R) (Drug
Reprofiling Platform(R):開発保留化合物の新規適応探索)及び国内外の製薬会社や大学などとの新規化合物共同研究によって、開発パイプラインを充実させています。同社は将来の自販体制確立に向けて営業部門の立ち上げにも着手しました。また同社は、過去10
年以上にわたって技術移転事業を展開してきており、そこで培った広範な世界的ネットワークを有しています。
ーーー
2015/2/21 そーせい
英国へプタレス社の株式取得(子会社化)に関するお知らせ
当社は、2015 年2月20 日(ロンドン時間)開催の取締役会において、英国Heptares
Therapeutics (へプタレス・セラピュティクス、英国ハートフォードシャー<www.heptares.com>)の全株式を取得し連結子会社とすることを決議し、同社の全株式を最大400
百万米ドルを対価として取得いたしましたので、下記のとおりお知らせいたします。
1. 株式の取得の理由
当社グループにおける現在の主たる収益源は、ノバルティス社に導出しているCOPD
(慢性閉塞性肺疾患:Chronic Obstructive Pulmonary Disease)治療薬である「シーブリ」および「ウルティブロ」のマイルストンおよびロイヤリティ収入ですが、さらなる企業価値の向上を目指すべくパイプラインの強化や新たな事業拡大を図り、この度へプタレス社の買収を実施しました。本買収により、当社は「日本発の世界トップバイオ企業になる」というビジョンをより迅速に達成できると期待しております。
へプタレス社は、英国のMRC Laboratory of Molecular Biology およびNational Institute of Medical
Research の研究成果を事業化するべく、2007 年に設立され、医薬品ターゲットとして期待の大きい、G
タンパク質共役受容体(GPCR)に作用する薬剤を創出する世界で最も進んだ独自の技術(StaR®)を有するバイオ企業です。同社は既に複数の著名な製薬企業との創薬共同研究契約を締結しており、開発の進捗に応じたマイルストン・ロイヤリティ収入を受領できることになっております。今回の買収により、当社グループの予測する2019
年の収益が3倍に近い水準まで伸び、それ以降も持続的に伸張し続けることが期待されます。
当社グループの中長期戦略の実現においてHeptares
社は極めて重要な役割を果たし、開発パイプラインの拡充や開発体制、グローバルな開発力、経営体制の強化のみならず、同社のパイプラインが2026
年以降の当社グループの収益の柱になると期待しております。
<本買収による当社への貢献>
① COPD 治療薬の特許が切れる2026 年以降の収益を生み出せるドラッグディスカバリー技術
ヘプタレス社は自社開発のみならず、独自のドラッグディスカバリー技術を基に、ノバルティス社、アストラゼネカ社、武田薬品工業株式会社等の世界トップレベルの製薬企業と提携契約を締結しており、既にマイルストン収入が発生しております。今後上市に至った場合には当該提携契約によるロイヤリティ収入が、COPD
治療薬の特許切れを迎える2026 年以降の収益の柱となります。
② 高収益パイプラインの拡充
へプタレス社の保有する独自技術は新規医薬品を効率的に多数創出することが可能であり、それらの自社研究開発の推進、または他社への導出を図ることで短期的な収益確保か
ら、長期的な収益基盤の構築まで、網羅的なポートフォリオ戦略が実現可能となります。
<へプタレス社のパイプライン>
| 開発プログラム
|
適応 |
開発段階 |
| ムスカリン受容体M1作動薬 |
アルツハイマー病、
認知障害 |
第Ⅰ相臨床試験 |
| M4 or M1/M4デュアル作動薬 |
統合失調症、
精神障害 |
前臨床試験 |
| アデノシン受容体2A 拮抗薬 |
注意欠如・多動性障害 |
前臨床試験終了、
IND(治験計画届出書)申請中 |
| CGRP 受容体拮抗薬
|
偏頭痛治療および予防 |
前臨床試験 |
| GPR39 作動薬 |
糖尿病、膵島β 細胞保護 |
前臨床試験 |
| GLP-1 作動薬
|
糖尿病 |
前臨床試験 |
本買収後の当社グループのパイプラインは、上記開発品に加え、ノバルティス社に導出済みのCOPD
治療薬「シーブリ」および「ウルティブロ」(欧州、日本等において上市済み、
米国において承認申請中)、SO-1105(第Ⅲ相臨床試験中)、および開発早期段階にある4品目の、全13 品目に拡充されます。
③ 開発体制の強化
本買収により、当社の日本での開発ノウハウと実績に加え、欧州と米国でのヘプタレス社のノウハウとネットワークが加わり、開発の体制の強化やそれぞれの地域の医薬品規制へ
の対応能力が強化されることになります。
また、欧米での開発や商業化の豊かな経験を持つ同社幹部が当社グループの一員として、新しい体制を支えていきます。
④ ドラッグディスカバリー基盤技術の獲得による、シーズ探索手法の強化
本買収により、当社の子会社である株式会社アクティバスファーマが保有する難溶性低分子医薬品のナノ粉砕化に関する独自の新規製剤技術(APNT)や、2014 年12
月に子会社化し
たJITSUBO 株式会社が保有している新規のペプチド合成技術(Molecular HivingTM)および新たなペプチド立体構造の改変技術(PeptuneTM)の新規ペプチド創薬基盤技術に加え、へ
プタレス社保有のドラッグディスカバリー基盤技術(StaR®)を獲得し、今後さらなるパイプラインの拡充とそれによる企業価値の向上が見込まれます。
また、基盤技術間のシナ
ジー効果も期待できます。
<統合後のマネジメント体制および組織>
本買収完了後に、当社グループの取締役兼代表執行役社長の田村眞一のもと、ヘプタレス社は当社の子会社として存続し、マルコム・ウェイアが引き続きCEO
として、国際的な研究開
発事業を率います。当社グループの社外取締役のデクラン・ドゥーガンおよびピーター・ベインズがヘプタレス社の取締役として当社グループから派遣されます。ヘプタレス社のCEO
のマルコム・ウェイアが当社の執行役副社長として就任します。
2. 異動の方法
当社は、へプタレス社の株主とのAgreement for the Sales and
Purchaseにより2015年2月20日付で既存株主より普通株式21,213,303株を取得し、その対価として180百万米ドルおよびヘプタレス社にて将来発生するマイルストンまたはロイヤリティ収入の額に応じて支払う条件付き対価最大220百万米ドル、合計最大400百万米ドルを支払います。これにより、ヘプタレス社は当社の連結子会社となります。
2005.07.25 チッソ
産学共同研究の成果を事業化
検査薬、診断薬材料の新会社を設立
http://www.chisso.co.jp/info/pres/pres050725.html
チッソ株式会社(本社:東京都中央区、社長:岡田俊一)は、神戸大学との共同研究の成果である熱応答性磁性ナノ粒子に関し、同大学工学部教授近藤昭彦氏と共同で事業会社「マグナビート株式会社(英名:Magnabeat
Inc.)」を設立いたします。
マグナビート株式会社は、熱応答性磁性ナノ粒子(商品名:Therma-Max)の販売を行うとともに、神戸大学、チッソ(株)その子会社であるチッソ石油化学(株)の協力のもと、市場開発、用途開発、技術面におけるユーザーサポート及び検査診断システムや診断薬材料の開発を実施いたします。
【新会社の概要】
会社名: マグナビート株式会社
英名:Magnabeat Incorporated
本 店: 兵庫県神戸市灘区(神戸大学内)
事業所: 千葉県市原市(チッソ石油化学(株)五井研究所内)
代表者: 代表取締役 大西 徳幸
(現チッソ石油化学(株)五井研究所主任研究員、本年7月29日就任予定)
役 員: 取締役 近藤 昭彦 他2名
資本金: 30百万円
株 主: チッソ(株) 95%、 近藤昭彦 5%
設 立: 2005年7月
従業員数:当初5名程度
事業概要:熱応答性磁性ナノ粒子の販売、市場開発、用途開発、技術サポート及び検査診断システムや診断薬材料の開発・研究
2005年6月24日/日経産業新聞
三九本草坊医薬、「三九製薬」に社名変更
中国の製薬大手・三九企業集団(広東省)の日本法人、三九本草坊医薬(東京・新宿、西村一郎会長)は漢方生薬を使ったサプリメント(栄養補助食品)の通信販売や医薬品の原料供給事業へ参入する。2005年3月期の売上高は15億円だが、06年3月期は30億円へ倍増を目指す。
きょう24日に開く株主総会では経営体制を刷新。西村会長が社長を兼務し、社名は「三九製薬」に変更する。
http://www.999jp.co.jp/home/corporate_profile/999jp-profile.html
日本経済新聞 2005/7/29
伊藤忠とアルフレッサ 中国で医薬品卸 現地製薬最大手三九と合弁
伊藤忠商事と医薬品卸第三位アルフレッサホールディングスは中国の製薬最大手三九企業集団と合弁で、外資として初めて中国で医薬品卸事業に参入する。三九企業集団の日本法人が広東省に設立した卸会社に8月中に各15%を出資し、10月から同社を通じ日本の医薬品を中国全土で卸売りする。急成長する中国市場に足場を築くとともに、中国経由で東南アジア諸国連合、(ASEAN)にも輸出する。
三九企業集団の日本法人、三九製薬は医薬品と化粧品の輸出入、中国全域での卸、小売事業を手掛ける免許を中国政府から取得。5月に広東省に「日美健薬品(恵州)公司」を全額出資で設立した。8月中に100万米ドルから600万ドルに増資する計画で、伊藤忠とアルフレッサがそれぞれ15%出資する。
2005年8月2日 ロート製薬
京都府・学研都市に最新設備を誇る大規模研究所を取得
機能性化粧品や食品分野の強化を目的に
先端の生命科学領域でのコラボレーションを推進します。
http://www.rohto.co.jp/company/news/release/050802.htm
ロート製薬株式会社(本社:大阪市、社長:山田邦雄)は、開発戦略をさらに発展させるために、7月20日付で、バイエル薬品株式会社(本社:大阪市、社長:栄木憲和)が所有する研究所(京都府 木津町)取得に関する契約を締結しましたのでお知らせ致します。
この研究所の取得により、ヘルスケア分野の技術基盤強化をはじめ、抗老化や予防領域への取組み、ベンチャー企業とのコラボレーション、国内外研究者との共同研究の推進を図るなど、ヘルス&ビューティー分野における総合的な研究体制の構築を図っていきます。
◆新研究所の概要
所在地: 京都府相楽郡木津町州見台6丁目5番地1-3
敷地面積: 48,399m2(約14,640坪)
建築面積: 6,862m2(約2,076坪) 地下1階付5階建(A、B、C、E棟)、地下1階付3階建(D棟)
延床面積: 22,072m2(約6,677坪)
日本経済新聞 2005/8/3
ロート、中国で大衆薬開発 医科大学と合弁
合弁会社は中国協和医科大学(北京市)と設立する。資本金は明らかにしていないが、ロートが過半を出資する。北京市内に拠点を設け、両者から研究者を派遣する。当面は風邪薬や胃腸薬、ビタミンなどを主な研究対象にする。
1991年に広州に工場を設立後、点眼剤やスキンケアを現地で製造・販売してきた。
2005/8/4 日本経済新聞
エーザイ、欧州に製剤拠点 2008年めど 50億円投じ製販一貫
エーザイは2008年をめどに欧州で薬剤生産を始める。場所は未定だが、研究所のある英国などを軸に検討する。投資額は約50億円で、主力の中枢神経系やガンなどの新薬を生産する。同社の日米事業の売上高はそれぞれ2千億円を超えるが、欧州は400億円弱にとどまっており、生産体制の強化で早期に1千億円超に引き上げる。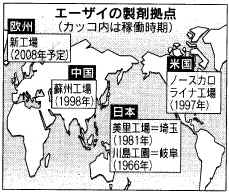
新工場では、鹿島事業所(茨城県神栖市)でつくった原薬を、錠剤などに加工、包装する工程などを置く。
2005/08/24 クラレメディカル
創傷被覆材「クラビオ(R)」の製造技術ライセンス供与について
http://release.nikkei.co.jp/detail.cfm?relID=108583&lindID=4
クラレメディカル株式会社(本社:東京都千代田区、社長:堀井秀夫以下クラレメディカル)と、光洋産業株式会社(本社:東京都千代田区、社長:舟山聡一以下光洋産業)とは、8月23日、クラレメディカルが開発した創傷被覆材(*)の製造技術を光洋産業にライセンス供与することに合意しましたのでお知らせします。(*)特定保険医療材料
【クラレメディカル株式会社】 http://www.kuraray.co.jp/Medical/
社 長:堀井秀夫
本社所在地:東京都千代田区大手町1-1-3 TEL 03-6701-1700(代表)
資本金:25億円(2005年3月末株式会社クラレ100%出資)
事業内容:メディカル関連製品の開発・製造・販売
売上高:121億円(2005年3月期)
【光洋産業株式会社】 http://www.koyoweb.com/
社 長:舟山聡一
本社所在地:東京都千代田区鍛冶町1-9-9 TEL 03-3252-1703(代表)
資本金:1億2千万円(2005年2月末)
事業内容:工業化学製品の製造・販売、メディカル関連製品の輸入・製造・販売
売上高:102億円(2005年2月期)
平成17年8月30日 シミック/エスエス製薬
シミック株式会社とエスエス製薬株式会社 子会社株式譲渡契約を締結
http://www.cmic.co.jp/ir/pdf/20050830_2.pdf
シミック株式会社(本社:東京、社長:中村
和男、以下「シミック」)とエスエス製薬株式会社(本社:東京、社長:羽鳥
成一郎、以下「エスエス製薬」)は、平成17年8月30日をもって、エスエス製薬の連結子会社である海東エスエス製薬株式会社(本社:韓国、社長:金鍾喆)の株式譲渡契約を締結いたしましたので、下記のとおりお知らせいたします。
1.株式譲渡の背景及び目的
海東エスエス製薬株式会社は、韓国において医薬品の製造を行っており、技術専門性の高さとコストパフォーマンスの良さを特長としております。シミックは、海東エスエス製薬株式会社を傘下に収めることにより、臨床試験支援事業において開発から製造、マーケティング、営業までの全ての過程の支援業務が可能となります。また、シミックは2005年4月改正薬事法の施行に伴い、製造受託の需要が拡大すると予測しており、製造受託の業務拡大、コンサルティング機能の強化、新規顧客の開拓が期待できると考え、株式の取得を決定いたしました。エスエス製薬は、コンシューマヘルスケア事業への経営資源の集中の方針のもと、子会社戦略の見直しを行った結果、よりふさわしいビジネスパートナーの下において、今後海東エスエス製薬株式会社の事業を発展させることが望ましいものと考え、株式の譲渡を決定いたしました。
2.方法
海東エスエス製薬株式会社の発行済普通株式335,437株(90%)をシミックがエスエス製薬から取得
3.当該子会社の概要
(1) 商号 海東エスエス製薬株式会社
(2) 代表者 金 鍾喆
(3) 所在地
韓国京畿道富川市遠美区陶唐洞157-3
(4) 設立年月日 昭和 48年9月1日
(5) 事業の内容 医薬品の製造
(6) 決算期 12月31日
(7) 従業員数 32名(平成17年8月8日現在)
(8) 資本金 3,727百万ウォン
(9) 発行済株式総数 372,708株
(10)出資比率
エスエス製薬株式会社(所有割合 100%)
(11)総資産及び業績
| |
平成15年12月期 |
平成16年12月期 |
売上高
|
3,313百万ウォン
|
3,272百万ウォン
|
売上総利益
|
1,091百万ウォン
|
820百万ウォン
|
営業利益
|
604百万ウォン
|
245百万ウォン
|
経常利益
|
666百万ウォン
|
798百万ウォン
|
総資産
|
8,849百万ウォン
|
8,423百万ウォン
|
株主資本
|
4,310百万ウォン
|
4,498百万ウォン
|
4.シミックの取得株式数、取得金額及び取得前後の所有株式の状況
(1)異動前の所有株式数 0株(所有割合0%)
(2)取得株式数 335,437株(取得価額
340百万円)
(3)異動後の所有株式数 335,437株(所有割合
90%)
5.日程 平成17年8月30日
株式譲渡契約書締結・株式譲受日
【シミック株式会社】
設立 : 昭和60年3月14日
資本金 : 3,081百万円
所在地 : 東京都品川区西五反田7丁目10番4号
代表者名 : 代表取締役会長兼社長 中村 和男
事業内容 : CRO事業(医薬品開発受託)
【エスエス製薬株式会社】
設立 : 昭和2年10月29日
資本金 : 10,162百万円
所在地 : 東京都中央区日本橋浜町2丁目12番4号
代表者名 : 代表取締役社長 羽鳥 成一郎
事業内容 :
医薬品、医薬部外品、医療用具、化粧品、食品等の製造・販売
2005/9/12 株式会社メディビック メディビック概要
財団法人かずさディー・エヌ・エー研究所との新薬開発等支援事業の共同開発開始のお知らせ
http://www.medibic.com/news/050912/20050912.pdf
この度、当社は、財団法人かずさディー・エヌ・エー研究所(千葉県木更津市、理事長
大石道夫、以下、「かずさDNA 研究所」という)と共同事業開発に関して契約を締結いたしましたのでお知らせします。
今回の契約は、かずさDNA
研究所の研究成果物を用いて、分子機能解析や新薬候補化合物探索等に関する研究支援事業を行うことを目的としております。
かずさDNA
研究所は、哺乳動物や植物の遺伝子研究のパイオニアであり、医薬学研究機関や医薬品産業界など国内バイオ産業を振興するDNA基礎研究を中心とした世界屈指の研究所の一つです。同研究所は、世界で公表されているヒト長鎖cDNA
の過半数以上を発見しデータベース化を行っているほか、ラン藻ゲノムやシロイヌナズナのゲノムの解読にも多くの成功を収めており、これらの遺伝子情報データベースや研究開発シーズなどが、世界の多くの研究者に配布され利用されています。
<ご参考>
かずさDNA 研究所の概要
名 称 :
財団法人かずさディー・エヌ・エー研究所
所在地 :
千葉県木更津市かずさ鎌足2丁目6番地7
電 話 : 0438-52-3900
代表者 : 理事長 大石 道夫
主な事業 : DNA の構造解析研究 、DNA
の構造解析技術に関する研究
DNA の機能等に関する研究、DNA
に関するデータ等の蓄積及び提供等
URL : http://www.kazusa.or.jp
名称
財団法人 かずさディー・エヌ・エー研究所
沿革
平成3年03月04日 民法第34条に基づく公益法人として設立(通商産業大臣許可)
平成4年02月06日 特定公益増進法人の証明を受ける。
平成5年06月24日 通商産業省及び科学技術庁の共管となる。
平成6年10月26日 研究所開所
基本財産 48億18百万円
目的
遺伝物質の本体であるDNAの構造の解析研究、DNAの構造の解析技術に関する研究、DNAの機能等に関する研究並びにDNAに関するデータ等の蓄積及
び提供等を行うことにより、
新しい産業分野の創出や産業構造の高度化及び科学技術の振興を促し、人類の福祉に貢献することを目的としています。
主要事業
(1)DNAの構造の解析研究
(2)DNAの構造の解析技術に関する研究
(3)DNAの機能等に関する研究
(4)DNAに関するデータ等の蓄積及び提供
(5)DNAの研究に関する人材の育成
(6)DNAの研究に関する普及啓発
(7)DNAの研究に関する内外関係機関等との交流及び協力
(8)前各号に掲げるもののほか、本財団の目的を達成するために必要な事業
2005年9月15日 ロート製薬
機能性食品素材開発のバイオベンチャー企業と共同開発ならびに資本提携に合意しました。
http://www.rohto.co.jp/company/news/release/050915.htm
ロート製薬株式会社(本社:大阪市、社長:山田邦雄)は、機能性食品素材開発のバイオベンチャー企業である株式会社ファーマフーズ(本社:京都市、社長:金武祚、以下ファーマフーズ)と共同開発ならびに資本参加に関して合意し、2005年9月14日付で契約の締結を行いました。ファーマフーズは、“免疫・老化・神経”の分野における機能性素材の開発力に優れたバイオベンチャー企業です。今回の締結により、アイケア、スキンケアに続く第3の柱の事業として当社が注力する機能性食品の開発スピードをさらに加速させてまいります。
| 2.
共同開発の主たる内容 |
| |
1. |
当社は、鶏卵抗体技術をベースに、ファーマフーズとの間で新しい機能性食品素材、医薬品素材の共同開発を行います。当社はファーマフーズへ医薬品・診断薬等に関する情報提供を行い、両社のビジネス展開を拡大していく予定です。 |
| |
2. |
本契約に基づく研究開発は、7月に取得契約しました木津新研究所内の共同開発室において実施する予定です。
|
3. 資本参加の内容
資本参加は、2005年9月15日に、ファーマフーズの普通株式1,000株(発行済株式総数に対する割合:2.3%)を第三者割当増資にて引受する予定です。本資本参加により共同開発の積極的な推進を図るとともに両社のさらなる企業価値の向上を図ってまいります。
ご参考
| 【ファーマフーズ会社概要】
http://www.pharmafoods.co.jp/ |
| |
代表者 |
|
金武祚(キム・ムジョウ) |
| |
所在地 |
|
京都市南区吉祥院石原堂ノ後西町24-5 |
| |
設立 |
|
1997年9月12日 |
| |
売上高 |
|
705百万円(2005年7月期) |
| |
資本金 |
|
384百万円(今回増資後) |
| |
従業員数 |
|
45名(2005年4月現在) |
| |
事業内容 |
|
機能性食品素材の開発・販売 |
| |
主な事業所 |
|
本社および東京事務所 |
| |
|
|
|
| 【ファーマフーズの沿革】 |
| |
1997年 9月 |
|
設立 |
| |
1999年 11月 |
|
通産省創造的事業活動促進法 認定企業 |
| |
同年 12月 |
|
京都ベンチャー創出支援事業に関わる投資先企業に採択 |
| |
2000年 6月 |
|
京都府創造技術研究開発費
補助金交付
財)食品産業センターベンチャー育成技術開発支援事業対象企業に採択 |
| |
同年 10月 |
|
中小企業総合事業団
革新促進事業企業に採択
さくら銀行
さくらベンチャー育成基金に採択 |
| |
2001年 5月 |
|
食品産業センター地域新生・食品産業活性化技術開発支援対象企業に採択 |
| |
2002年 3月 |
|
第1回日本バイオベンチャー大賞近畿バイオインダストリー振興会議賞 |
| |
同年 7月 |
|
近畿経済産業局
創造技術研究開発費 補助金交付
経済産業省新エネルギー・産業技術総合開発機構(NEDO)補助事業企業採択 |
| |
同年 9月 |
|
中小企業総合事業団
課題対応新技術研究開発事業に採択 |
| |
2003年 4月 |
|
近畿経済産業局
創造技術研究開発費 補助金交付 |
| |
2004年 2月
|
|
財団法人京都産業21
京都中小企業技術大賞受賞 |
| |
同年 11月 |
|
京都市ベンチャー企業目利き委員会
Aランク企業認定 |
| |
2005年 3月 |
|
Japan Venture Award
2004 委員長特別賞 受賞 |
平成17年9月26日
メディビック
Bunstatグループ(中国)との事業提携に関するお知らせ
http://www.medibic.com/news/050926/20050926.pdf
この度、㈱メディビックの100%出資子会社である㈱メディビック・アライアンス(代表取締役社長:小林
光、本社:東京都千代田区)は、Bunstat
International Group Limited(所在地:香港、CEO:Huang Minjun、以下「Bunstat社」という。)と、事業において協力体制を確立するための事業提携を行うことで合意しましたのでご連絡いたします。
Bunstat社を中心とするBunstatグループは2002年以降、中国本土の90以上の病院で950室以上の手術室の設計および建築を手掛けてきた中国最大手の手術室設計・建築企業グループで、市場シェアの40%以上を占めています。Bunstatグループは、中国全土の病院に対して、ICU(集中治療室)、BCU(熱傷治療室)、BMTU(骨髄移植手術室)などの手術室の設計・建築および関連設備の提供を行っております。
<Bunstat社の会社概要>
商 号 :Bunstat International Group
Limited
所在地 :Suite 1904, Tower 6, The Gateway,
9 Canton Road, Tsimshatsui, Kowloon, Hong Kong
CEO
:Huang Minjun
設 立 :1986年6月
資本金 : HK$ 10,000,000 (2004年12月現在)
グループ従業員 : 267名(2004年12月現在)
事業内容 : 手術室等の設計、建築、設備販売
URL : http://www.bunstat.com/eng/main.html
<メディビック・アライアンスの概要>
設 立 : 2004年4月
本 社 : 東京都千代田区霞が関一丁目4番2号
代表者 : 代表取締役社長 小林
光(株式会社メディビック専務取締役)
資本金 : 6億6千万円(2004年12月期)
株主構成 : 株式会社メディビック100%
事業内容 :
ベンチャー企業への投資、投資事業組合運営管理業務、投資先企業への事業育成、
M&A
などフィナンシャルアドバイザリー業務、等
2005/9/29 参天製薬
中国現地法人設立に関するお知らせ
http://www.santen.co.jp/ir/jp/news/pdf/20050929.pdf
参天製薬株式会社〔本社:大阪市東淀川区/社長:森田隆和〕は、中国江蘇省工商行政管理局より営業許可を取得し、中国に現地法人「参天製薬(中国)有限公司」を、当社の100%単独出資により設立しました。
当社はこれまで中国において、北京、広州および上海に駐在員事務所をおき、医薬学術情報活動を積極的に展開するとともに、当社医療用眼科薬を日本から輸出し、現地代理店経由で販売を行ってまいりました。
今般設立した中国現地法人では、医療用眼科薬の開発、蘇州工業園区での工場新設ならびに自社販売網の構築を行い、拡大を続ける中国市場でさらなる当社製品と参天ブランドの浸透に努めます。
会社名: 参天製薬(中国)有限公司
Santen Pharmaceutical (China) Co., Ltd.
所在地: 江蘇省蘇州市蘇州工業園区三区
設立: 2005 年9 月21 日
操業開始: 2009 年1 月(予定)
資本金: 23 億円
出資比率: 参天製薬株式会社 100%
代表者: 董事長 森田 隆和〔参天製薬株式会社
代表取締役社長〕
事業内容: 医療用眼科薬の開発、製造、販売
全従業員数: 約200 名(操業開始時)
工場の概要(本社事務所含む):
敷地面積: 約30,000m2
建築面積: 約 7,700m2
予定工期: 着工 2006 年、竣工2007 年
生産能力: 約2000 万本/年
日本経済新聞 2005/9/28-29
号砲 医薬再編
統合に賭ける突破口 新薬開発、世界に照準
三共と第一製薬が28日、持ち株会社「第一三共」を設立し、国内2位グループの医薬品会社になる。10月1日には大日本製薬と住友製薬など準大手や中堅、医薬卸の間でも統合が相次ぐ。国内医薬市場が伸び悩む中、再編で突破口を探る動きが一気に加速する。
製薬関連企業の今秋の主な経営統合
|
新社名
(発足日) |
経営統合の形態 |
連結売上高 |
特徴 |
第一三共
(9月28日) |
三共と第一製薬が持ち株会社を設立
|
9,164
|
国内製薬会社の2位規模、
2007年4月に医薬事業を完全統合
|
大日本住友製薬
(10月1日) |
大日本製薬と住友製薬が合併
|
3,162
|
国内5位の規
模、
医薬情報担当者(MR)人数でも上位
|
あすか製薬
(10月1日)
|
帝国臓器製薬とグレラン製薬(東京都羽村市)が合併
|
307
|
泌尿器や消化器、産婦人科の領域に強み
|
メディセオ・パルタック
ホールティングス
(10月1日)
|
医薬品卸最大手のメディセオホ一ルディングスが
日用雑貨卸2位のパルタックを完全子会社化
|
20,520
|
医療用医薬品から大衆薬、日用品まで
幅広く取り扱い、医薬品卸で初の2兆円企業に
|
| (注)単位億円、連結売上高は統合前の2005年3月期の単純合計だが、パルタックのみ04年9月通期 |
踊り場の成長産業 難病治療薬
開発カギ
ファイザーの05年1-6月期の純利益は前年同期比28%減した。ワーナー・ランバートなど有力薬を持つ大手を相次いで統合し、04年までの5年間で最終利益は2.3倍に成長した勢いは衰え、工場の閉鎖や人員削減などリストラ計画を打ち出した。
ファイザーだけではない。米メルクは副作用問題で一時25億ドルを販売した消炎鎮痛剤の販売を中止。英グラクソスミスクラインは主力薬の特許切れで、04年の売上高が横ばい(為替調整べース)だった。
ブロックバスターが変調をきたしている。各国の規制当局の安全性に対する基準は厳しさを増し、薬剤費抑制の圧力も強まっている。新薬の発売ぺースは鈍り、研究開発費は膨れあがる。
04年の米医薬品市場の成長率は8%と、8年続いた2ケタ成長がとぎれた。日本の大手が再編で攻め込む海外市場は、巨大製薬会社ですら伸び悩むほど厳しさを増している。
| 世界大手の2004年の医薬品売上高 |
| 順位 |
メーカー名 |
売上高
(億ドル) |
研究
開発費
(億ドル) |
1
|
フアイザー(米)
|
461.3
|
76.8
|
2
|
サノフィ・アベンティス(仏)
|
346.8
|
54.0
|
3
|
グラクソスミスクライン(英)
|
330.3
|
54.7
|
4
|
メルク(米)
|
229.3
|
40.1
|
5
|
ジョンソン・エンド・ジョンソン(米)
|
221.2
|
36.4
|
6
|
ノバルティス(スイス)
|
215.4
|
42.1
|
7
|
アストラゼネカ(英)
|
208.6
|
38.0
|
8
|
ロシュ(スイス)
|
191.7
|
38.9
|
9
|
ブリストル・マイヤーズ・スクイブ(米)
|
154.8
|
25.0
|
10
|
ワイス(米)
|
139.6
|
24.6
|
11
|
イーライ・リリー(米)
|
130.5
|
26.9
|
12
|
アボット・ラボラトリ一ズ(米)
|
115.8
|
17.0
|
13
|
アムジェン(米)
|
105.5
|
20.3
|
14
|
武田薬品工業
|
88.7
|
13.7
|
15
|
べ一リンガー・インゲルハイム(独)
|
84.3
|
16.4
|
16
|
アステラス製薬
|
81.1
|
12.4
|
17
|
第一三共
|
73.2
|
14.1
|
(注)デンドライトジャパン調べ。第一三共など統合会社は単純合計で計算。
日本企業は05年3月期
|
平成17年10月3日 ニプロ
有機合成薬品工業㈱との業務提携について
http://www.nipro.co.jp/topics/051003.pdf
このたび、ニプロ株式会社は、医薬品事業分野において、有機合成薬品工業株式会社との間で、次のとおり業務提携をすることに合意しましたのでお知らせします。
2.提携業務の内容
(1)ニプロが開発、製造する医薬品に必要な原薬・中間体の開発、製造に関して、両者間で技術的な協力を行う。
(2)医薬品の一貫製造体制の構築に向け両者間で連携することにより、品質、コスト面での充実を図り、顧客サービスの一層の向上を図る。
(3)医薬品事業はもとより、その他の事業分野においても相互の発展のため業務上の協業を模索する。
日本経済新聞 2005/10/4
アンジェスMGと協力
ホソカワミクロン(粉体機械製造)医薬品開発のアンジェスMGが開発したアトピー治療薬を自社が手がけるナノ粒子に封入することに成功した。直径200ナノ(ナノは十億分の1)メートルの粒子に薬剤を封人することで、直接塗布するよりもより深く、皮膚に浸透する可能性があるという。薬理効果を確認するためアンジェス側が試験を実施する。
2005/10/3 アンジェス MG/ホソカワミクロン
ホソカワ粉体技術研究所がアンジェスMG
の核酸医薬をDDS 用ナノ粒子に封入成功
炎症性皮膚疾患を対象とした「核酸DDS
製剤」としての評価を開始
http://www.hosokawamicron.co.jp/main/1news/pdf/news20051003.pdf
ホソカワ粉体技術研究所は、アンジェスMGから、かねてより生体適合性かつ生体吸収性ナノ粒子の中にNFκB
デコイオリゴを封入したコンポジットナノ粒子を製作する研究を委嘱されていましたが、今回、その封入に成功致しました。
NFκB
デコイオリゴは、アンジェスMGが開発した核酸医薬で、皮膚疾患領域への応用として、アトピー性皮膚炎や乾癬に対する皮膚外用剤としての効果が期待されています。
アンジェスMGは、NFκB
デコイオリゴを皮膚内部に送達し、そのアトピー性皮膚炎等に対する治療効果を高めるべく、ホソカワ粉体技術研究所のDDS
技術の適用を図ったもので、今回、ナノ粒子への封入が成功したことにより、皮膚疾患への薬理効果の評価を開始致しました。
NFκB
デコイオリゴなどの水溶性核酸医薬品は、これまでPLGA
ナノ粒子に封入することが困難でしたが、ホソカワ粉技研が独自に開発した「表面修飾型PLGA ナノ粒子」を用いることで、ナノ粒子内部への封入と共に、ナノ粒子表面層への薬剤担持が可能となり、薬物送達効率の向上を図ることができるものと期待されます。
今回行われる炎症性皮膚疾患治療を目的とする核酸医薬の経皮DDS
製剤の事業化検討は、新しいナノバイオテクノロジーの可能性を拓くものであり、今後、タンパク質医薬、遺伝子・核酸医薬などの最先端医療技術への展開が期待されます。
日本経済新聞 2005/10/4
富士写が医療関連拡大 治験支援大手シミックと新会社
富士写真フイルムは臨床試験(治験)支援大手のシミックと提携し、ライフサイエンス(生命科学)事業を拡大する。共同で新会社を設立、シミックが持つ医薬品の治験ノウハウを生かし、医療機関向けの製品を本格販売する。治験が必要な試薬開発も進める見通し。富士写は写真フィルムで培った製造技術が活用できると見て、医療・健康関連の機器やサービスを提供する「ライフサイエンス事業」を成長事業に育てる方針だ。
新会社は「富士フイルム・シミックヘルスケア」で資本金は1億円。富士写が6割、シミックが4割出資した。シミックが持つ医薬品の治験ノウハウを富士写の新製品開発に生かす。医療・健康関連市場の調査も共同で進める。
日本経済新聞 2005/10/7
三菱重工 コニカミノルタと提携 医療機器で共同出資会社
三菱重工業は医療機器事業でコニカミノルタホールディングスと提携する。共同出資会社を設立し、三菱重工が開発したX線がん治療装置を販売するほか、コニカミノルタの診断装置技術を取り入れた新製品の共同開発にも乗り出す。提携を機に医療機器事業を新たな柱に育てる。
共同出資会社、MHIメディカルシステムズは資本金9600万円。三菱重工が50%、コニカミノルタの医療機器子会社であるコニカミノルタエムジーが20%、三菱商事、西華産業がそれぞれ15%出資し、11日に設立する。
2005年10月7日 三菱重工
放射線治療装置などの販売・サービス会社を設立
コニカミノルタエムジー、三菱商事、西華産業と合弁で
http://www.mhi-ir.jp/news/sec1/200510074402.html
1.会社概要
(1) 商 号:MHIメディカルシステムズ株式会社
(英文名:MHI Medical Systems, Inc.)
(2)
事業内容:医療機器の販売、保守・点検・修理サービス
(3) 設立年月日:平成17年10月11日
(4) 本社所在地:東京都港区三田三丁目11番36号
(5) 代表者 :石橋 明
(6) 資本金 :96百万円
(出資比率 三菱重工業 50%、コニカミノルタエムジー
20%、三菱商事 15%、西華産業 15%)
(7) 人 員 :11人 (常/非常勤で、保守サービス対応要員を除く)
2.各社概要
◇ 三菱重工業株式会社
所 在 地:東京都港区港南2-16-5
取締役社長:佃 和夫
◇コニカミノルタエムジー株式会社
所 在 地:東京都新宿区西新宿1-26-2 新宿野村ビル
取締役社長:谷田 清文
◇三菱商事株式会社
所 在 地:東京都千代田区丸の内2-6-3
代表取締役社長:小島 順彦
◇西華産業株式会社
所 在 地: 東京都千代田区丸の内3-3-1
新東京ビル
取締役社長: 藤本 守孝
朝日新聞 2005/10/9
医薬品卸、大手は4グループに再編
http://www.asahi.com/business/update/1009/004.html
医薬品卸の大手が、相次ぐ企業合併・買収(M&A)で4グループに再編された。ドラッグストアの増加に対応するため、化粧品卸など異業種との経営統合も進んでおり、規模のメリットをめざした医薬品卸業界の動きがさらに加速する可能性もある。
クラヤ三星堂など全国の卸10社を傘下に持つ最大手、メディセオホールディングスが1日、日用雑貨・化粧品卸大手のパルタックと経営統合。雑貨を含め幅広く扱うドラッグストアとの関係強化が狙いで、売上高は医薬品卸として初めて2兆円を超える見込みだ。
(株)メディセオホールディングスは、2005年10月1日、化粧品・日用雑貨品卸売業の(株)パルタックと経営統合し、株式会社メディセオ・パルタックホールディングスに商号変更いたしました。
2位のスズケンは塩野義製薬系の卸を合併するなどして売上高をこの5年で約1.5倍に増やした。3位のアルフレッサホールディングスも広島市の中堅卸を完全子会社化した。スズケンは10年度に、アルフレッサは07年度に売上高2兆円の達成をめざす。4位の東邦薬品も今年3月、全国の地域卸6社と業務提携している。
薬価引き下げを受け、納入先の病院や薬局からの値引き要求は強まっている。また、研究開発費の確保に懸命な製薬業界側はリベートなど卸への支援を抑えている。このため零細の卸企業の廃業も相次ぎ、日本医薬品卸業連合会によると、05年3月末の加盟社は142社と95年3月末の約半分まで減っている。
日本経済新聞 2005/10/19
バイオベンチャー新タイプ 創薬基盤技術型が台頭
高い技術力 独自医薬品候補も保有 製薬会社支援実績重ねる
日本のバイオベンチャーで新しいタイプの企業群が台頭している。完成間近の医薬品は持っていないが、創薬に直結する技術を持つ「創薬基盤技術型」だ。これまでは医薬品を開発する「創薬型」と解析機器などを販売する「研究支援型」か中心だった。中間型ともいえる企業群は製薬会社との取引実績を積み重ね、バイオ市場の成長を引っ張る可能性がある。
たんぱく質解析を手がけるメディカル・プロテオスコープ(MPS)
会社名:
株式会社メディカル・プロテオスコープ http://www.medicalproteoscope.com/
Medical ProteoScope Co. Ltd.
代表取締役社長: 松山 哲人
所在地: 東京都新宿区西新宿2-6-1新宿住友ビル17F
設立日 :2002年11月18日
業務内容:
疾患特異的な発現蛋白質の同定と解析
従業員数: 18名 (2005年2月現在)
たんぱく質の立体構造を解析し、病気の発現を抑える化合物を効率よく探し出す技術を持つファルマデザイン
商号 株式会社ファルマデザイン http://www.pharmadesign.co.jp
PharmaDesign, Inc.
本社所在地 東京都中央区八丁堀2-19-8
長谷工八丁堀ビル
設立年月日 1999年1月25日
代表者 代表取締役社長 古谷 利夫
資本金 447百万円
発行済株式数 28,700株
従業員数 27名(臨時雇用等含む)
主な事業
バイオインフォマティクス、合理的なドラッグデザインを融合させた創薬開発及びライセンスアウト
バイオインフォマティクス、合理的なドラッグデザインに関する受託研究
データベース、ソフトウェア、ライブラリ等創薬研究ツールの販売
日本経済新聞 2005/10/21
韓国、ES細胞を世界に提供
再生医療 本命見えず クローン技術使わぬ方法も
国内の主な再生医療研究
| 材料となる細胞 |
手がけている主な機関 |
作製する細胞 |
開発段階 |
| ヒトES細胞 |
京都大学・田辺製薬 |
血管 |
ヒト細胞で基礎研究 |
| 慶応大学 |
神経 |
〃 |
| 理化学研究所 |
神経 |
〃 |
| 東京大学 |
造血細胞 |
〃 |
| 患者細胞と融合したES細胞 |
リプロセル |
骨、神経、血管など |
動物細胞で基礎研究 |
| 患者の脂肪にある幹細胞 |
名古屋大・協和発酵 |
脂肪、骨 |
ヒト細胞で基礎研究 |
| 患者の骨髄にある幹細胞 |
国立循環器病センター |
血管、心筋 |
臨床研究 |
| 大阪大学 |
血管、心筋 |
〃 |
| 信州大学 |
血管 |
〃 |
| 埼玉医科大学 |
血管 |
〃 |
日本経済新聞 2005/10/21
後発医薬品追い風期待 医療制度改革、普及促す
東和薬品 営業担当400人に
日本調剤 薬局自ら開発も
特許切れ成分を使う低価格の後発医薬品市場の拡大をにらみ、専業メーカーと調剤薬局が販売体制の拡充や研究開発の強化に乗り出している。大手病院の採用が広がりつつあるのに加え、医療費削減を急ぐ厚生労働省も19日発表した医療制度改革試案で後発医薬品の普及を後押しする。各社は製品の信頼性や効率を高め、病院や薬局への売り込みに拍車をかける。
市場成長でも競合激化 再編・淘汰避けられず
主な国内の後発薬メーカーの売上高
(単位億円、富士製薬工業のみ単独業績) |
東和薬品(05年3月期)
|
247
|
沢井製薬(05年3月.期)
|
232
|
日医工(04年11月期)
|
182
|
富士製薬工業(04年9月期)
|
96
|
|
2005/10/26 ノバルティス
ニュートリション事業部の分社化について
http://release.nikkei.co.jp/detail.cfm?relID=114234&lindID=4
ノバルティスは、2006年1月1日付でニュートリション事業部を分離独立させ、ノバルティス ニュートリション株式会社を設立します。
日本におけるノバルティスのニュートリション事業部は、ノバルティス社(本社:スイス・バーゼル市)によるミードジョンソンの成人向け医療用栄養食品事業の買収に伴い、2004年2月14日付で設立されました。
■ 新会社の概要
社名: ノバルティス ニュートリション株式会社(Novartis Nutrition K.K.)
(ノバルティスホールディングジャパン株式会社の100%子会社)
本社所在地: 東京都港区西麻布4丁目16-13 西麻布28森ビル
代表取締役社長: 志道 保(しじ たもつ)
社員数: 約100人
事業内容: 医療用栄養食品(医療機関・介護施設向け栄養食品)の製造・販売
主要製品:
アイソカル(R)・アルジネード(TM)、アイソカル(R)・RTU、アイソカル(R)・プラス、アイソカル(R)・2K、アイソカル(R)・プディング、アイソカル(R)・ジェリーPCF、アイソカル(R)・ジェリー“くりん”
2005/10/31 メルク
ドイツメルク
日本における医薬品事業の再編を発表
http://release.nikkei.co.jp/detail.cfm?relID=114620&lindID=4
メルク株式会社(本社東京、社長 クラウス・ディール)及びメルク・ホエイ株式会社(本社大阪、社長 同)の親会社であるMerk
KGaA(本社ドイツ ダルムシュタット市、社長 ベルンハルト・ショイブレ)は10月31日、日本における医薬品事業の再編計画を発表しました。2006年4月にメルク株式会社の医薬品事業部とジェネリック医薬品の拠点であるメルク・ホエイ株式会社を統合し、新会社メルクファーマ株式会社(本社東京)を設立いたします。
メルク・ホエイ株式会社は1950年に保栄薬工として発足し、1998年にメルク・グループの傘下に入った後、日本におけるメルク・グループのジェネリック医薬品事業を担ってきました。
平成17年11月11日 日本ケミファ
子会社の異動及び業績予想の修正に関するお知らせ
http://www.chemiphar.co.jp/nc/news/20051111-3.pdf
当社は、平成17年11月11日開催の取締役会において、当社の子会社である日本薬品工業株式会社の株式を譲渡することを決議いたしました。また、この株式譲渡に伴い、本年8
月5 日の第1 四半期財務・業績の概況発表時に公表した平成18
年3 月期(平成17年4月1日~平成18年3月31日)の業績予想を下記のとおり修正いたしましたのでお知らせいたします。
1.株式譲渡の理由
当社は、ジェネリック医薬品市場で世界のトップ水準にあるランバクシー社と平成14
年9 月に当社子会社の日本薬品工業株式会社に対する10%資本参加を含む包括的業務提携を締結し、以来、同社との提携関係を着実に構築してまいりました。
この度、同社との提携関係を更に強固なものとし、同社の持つ優れた技術を活用したジェネリック医薬品等の更なる市場導入により、当社ジェネリック医薬品の充実(品揃え)を図るとともに、開発パイプラインの強化をより一層進めるため、当社の保有する日本薬品工業株式会社の発行済株式128,000 株(発行済株式総数の40%)を同社に譲渡することといたしました。これにより、同社の日本薬品工業株式会社に対する出資比率は50%となります。
なお、今般の株式譲渡に伴い、従来、連結子会社でありました日本薬品工業株式会社は当連結会計年度下半期において連結の範囲から除外し、持分法適用の関連会社となります。
2.譲渡する子会社(日本薬品工業株式会社)の概要
(1)商号 日本薬品工業株式会社
(2)代表者 代表取締役社長 嶋田 隆
(3)所在地 東京都千代田区岩本町二丁目2 番3
号
(4)設立年月日 昭和35 年8 月4 日
(5)主な事業の内容 医薬品の製造販売
(6)決算期 3 月31 日
(7)従業員数 57 名(平成17 年10 月31 日現在)
(8)主な事業所 茨城工場(茨城県稲敷市伊佐部1281
番地)
(9)資本金 160 百万円
(10)発行済株式総数 320,000 株
(11)大株主構成及び所有割合 平成17年10月31日現在
| 氏名又は名称 |
所有株式数 |
所有割合 |
| 日本ケミファ株式会社 |
181,440 株 |
56.7% |
| ジャパンソファルシム株式会社 |
63,880 株 |
20.0% |
| 山口 一城 |
38,680 株 |
12.1% |
| ランバクシー・ネザーランズ
B.V. |
32,000 株 |
10.0% |
(12)最近事業年度における業績の動向 略
| 3.株式の譲渡先 |
| (1)商号 |
|
ランバクシー・ネザーランズ
B.V.(Ranbaxy Netherlands B.V.) |
| (2)代表者 |
|
ラム・ラマスンダー(Mr.
Ram S. Ramasundar) |
| (3)本店所在地 |
|
オランダ国アムステルダム、1012
KK、ロキン 55
(Rokin 55, 1012 KK Amsterdam, The Netherlands) |
| (4)主な事業の内容 |
|
医薬品及び医薬関連品の輸出入、購入、販売等 |
| (5)当社との関係 |
|
同社は包括的業務提携をしているランバクシー・ラボラトリー・リミテッド社の
100%出資子会社で、海外への投資を担っている会社であります。 |
| |
| 4.譲渡株式数、譲渡価額及び譲渡前後の所有株式の状況 |
| (1)異動前の所有株式数 |
|
181,440 株 (所有割合56.7%) |
| (議決権の数
181,440 個) |
|
|
| (2)譲渡株式数 |
|
128,000 株 (譲渡価額1,800
百万円) |
| (議決権の数
128,000 個) |
|
|
| (3)異動後の所有株式数
|
|
当社所有 53,440 株 (所有割合16.7%、議決権の数
53,440 個) |
| |
|
借株(注) 106,560 株 (所有割合33.3%、議決権の数
106,560 個) |
| |
|
合計 160,000 株 (所有割合50.0%、議決権の数
160,000 個)
(注)株券消費貸借契約による借り受であります。 |
5.日程
平成17 年11 月11 日 取締役会決議
平成17 年11 月11 日 譲渡契約締結
平成17 年11 月18 日 株券引渡し日(予定)
2005/11/25 カネボウ株式会社
中国における販売会社の設立について
http://www.kanebo.co.jp/files/051125_01/051125yakuhin.pdf
当社は、中国における保健食品(日本の特定保健用食品に相当)、医薬品、漢方薬のエキス粉末等の販売会社の設立に関して、中国医薬集団総公司傘下の中国薬材集団公司及び中国医薬対外貿易公司と合意に達し、本日(11
月25 日)、中国北京市にて3社による調印式を行いましたので、お知らせいたします。
当社は、中国青島市にある合弁企業「青島華鐘製薬有限公司
」(出資比率:当社50%、中国薬材集団公司25%、中国医薬対外貿易公司10%、青島国風集団薬材有限責任公司15%)
で、漢方薬のエキス粉末等の中間体を日本向けに製造しており、これまで中国は原料供給拠点としての位置づけでありました。
<新会社の概要及び事業内容>
1.社 名 「華鐘高科医薬(北京)有限公司」
2.設立時期 2006 年3 月(予定)
3.所在地 中国北京市
4.資本金 100 万米ドル
出資構成:カネボウ株式会社65%、中国薬材集団公司25%、中国医薬対外貿易公司10%
5.事業内容
保健食品、医薬品、漢方エキス粉末並びに関連製品の販売、輸出入及びこれら製品に関する
コンサルティングサービスの提供その他関連業務。
<参考>
1.中国医薬集団総公司の概要
①設立時期 1998 年
②所在地 北京市海淀区知春路20 号
③董事長 鄭鴻
④事業内容
中国中央政府が管理する医薬研究、生産、サービス貿易
2.中国薬材集団公司の概要
①設立時期 1955 年
②所在地 北京市宣武区広安門外大街248 号
③総経理 李光甫
④事業内容
生薬、エキス、漢方薬の研究開発、製造・販売
3.中国医薬対外貿易公司の概要
①設立時期 1981 年
②所在地 北京市海淀区知春路20 号
③総経理 厳兵
④事業内容 医薬関連製品の輸出入
4.青島華鐘製薬有限公司の概要
①設立時期 1988 年
②資本金 10 億円
③所在地 山東省青島市重慶南路202 号
④総経理 加藤嘉昭
⑤事業内容 各種漢方薬の製造・販売
2005/11/29 萬有製薬
万有製薬、メルク社の事業再構築策の一環として一部組織を集約統合
http://www.banyu.co.jp/company/news/2005/1129merck.pdf
万有製薬株式会社(本社: 東京、代表取締役社長: 平手晴彦、以下、万有製薬) は、米国メルク社(Merck
& Co., Inc., Whitehouse Station, NJ, USA、以下、メルク) によるグローバルな事業再構築策、すなわち、グローバルベースでの効率向上ならびにコスト削減による競争力強化策の中で重要な役割を果たすべく、日本における一部業務の再編ならびに合理化を実施することを決定いたしましたので、お知らせいたします。具体的な施策は次の通りです。
● メルクのグローバル・サプライ戦略の一環を担うべく、岡崎工場(愛知県)を2006年末で閉鎖し、現在同工場で行っている抗生物質チエナム(R)の生産はメルクグループの他の工場に集約し、包装業務は妻沼工場(埼玉県)へ移管する
● 岡崎の合成技術研究所と妻沼の製剤研究所を2006年3月末に閉鎖し、現在両研究所で行っている前臨床開発業務をメルクグループの他の研究所に集約する。一部の業務はつくば研究所へ移管する
● 東京物流センターを2006年5月に閉鎖し、物流拠点を大阪に集約する
これに伴い、向こう1年間で約300名分のポジションを削減する予定です。今回の経営判断は、将来に向けた体質強化および戦力増強を主眼としたものであり、営業人員(医薬情報提供者)やマーケティング部門はさらに拡充していく方針です。
万有製薬はこれらの施策を通じて競争力を強化し、将来の長期的な成長に向けた基礎を築くことを目指します。
日本経済新聞 2006/1/24 沢井製薬発表
住商 沢井製薬子会社に出資
住友商事は23日、沢井製薬の全額出資子会社、メディサ新薬に資本参加すると発表した。1月末に実施する第三者割当増資を引き受け、住商グループで35%を出資する。特許切れ成分を使う後発医薬品を取り扱うメディサ新薬に対し、海外メーカーの技術仲介や販売ルート開拓で支援する。
住商が20%、住商子会社の住商メディケムが15%を出資する。出資額は両社合わせて12億2700万円。役員も派遣する。メディサ新薬は自前の販売ルートを持たず、新薬メーカーなどに販売している。
2006/1/23 沢井製薬
沢井製薬株式会社
子会社「メディサ新薬株式会社」による、
住友商事グループを割当先とする第三者割当増資実施のお知らせ
http://www.sawai.co.jp/press/2006/20060123.html
* 1.目的
今般の住友商事株式会社および住商メディケム株式会社への第三者割当増資によるメディサ新薬株式会社への資本参加により、メディサ新薬株式会社の既存事業の拡充および新規抗がん剤ジェネリック医薬品開発事業の円滑な立ち上げを目指して参ります。
*
2.メディサ新薬株式会社における第三者割当増資の概要
(1)発行株式 普通株式 3,230株
(2)発行価額総額 12億2,740万円
(3)払込期日 平成18年1月31日(予定)
(4)増資後の株主構成 沢井製薬株式会社 約65%
住友商事株式会社 約20%
住商メディケム株式会社 約15%
2006年1月24日 エーザイ
英国に欧州戦略拠点を設立
http://www.eisai.co.jp/news/news200603.html
エーザイ株式会社(本社:東京都、社長:内藤晴夫)の欧州統括子会社であるエーザイ・ヨーロッパ・リミテッド(本社:ロンドン、社長:土屋裕)は、このたび英国アーリントン社と欧州戦略拠点設立に向けた土地売買ならびに開発に関する覚書を締結いたしました。今後エーザイは、本用地に欧州における研究、臨床開発、生産、販売、欧州統括の各機能を集約し、欧州全域にわたる事業活動の中心となる戦略拠点を構築してまいります。
英国貿易投資総省 ファクトシート 2006年1月
参考資料 英国の医薬品・バイオテクノロジー産業の概要
日本経済新聞 2006/2/19
世界医薬大手 咋年の売上高
欧州勢伸び米社苦戦 武田は順位下げ14位
世界の製薬大手の2005年決算がほぼ出そろい、売上高を順調に伸ばす欧州企業と、苦戦気味の米上位の明暗が浮き彫りになった。日本勢では武田薬品工業の14位が最高で、第一三共は16位、アステラス製薬は17位に食い込んだ。大型医薬品の販売動向や特許切れ対策で順位が入れ替わる構図になっている。
日本経済新聞 2006/2/19 発表
富士写、医薬品に参入 創薬VBに出資 がん・糖尿病薬開発
富士写はペルセウスの第三者割当増資を引き受け、発行済み株式の22%を持つ筆頭株主になった。出資額は約10億円。ペルセウスは東大教授らの医薬品技術をもとに研究用試薬などを開発するベンチャーで2004年度の売上高は約3千万円。
富士写はペルセウスと共同で、がんや糖尿病の治療に使う副作用の少ない抗体医薬品の開発に取り組む。化学薬品子会社、富士写真フィルムファインケミカルの製造ラインを活用し、数年後に生産を始める。
ペルセウスプロテオミクス Perseus
Proteomics Inc. http://www.ppmx.com/
ペルセウスプロテオミクスは、東京大学
先端科学技術研究センター(駒場オープンラボ)のシステム生物医学ラボラトリー(LSBM)からタンパク質発現等に関する研究成果の技術移転を受け、LSBMが誇る世界最先端の分子生物医学分野のサイエンティストと臨床医とともに、がんや生活習慣病に対する抗体医薬品を始めとするバイオ医薬品やバイオマーカーを開発しています。
| 2001年2月 |
|
東京大学先端科学技術センターシステム生物医学ラボラトリーの技術を基盤として設立
|
| 2002年10月 |
|
抗核内受容体モノクローナル抗体を研究試薬として販売開始 |
| 2003年10月 |
|
ベンチャーキャピタルから、6億5,000万円を第三者割当増資により資金調達 |
| 2004年5月 |
|
動脈硬化マーカーとして期待されるPTX3診断薬キットの共同開発についてシミック株式会社と合意
|
| 2005年2月 |
|
シミック株式会社グループから、3億円を第三者割当増資により調達
|
2006/2/20 富士写真フイルム
富士フイルム 創薬ベンチャーのペルセウスプロテオミクスに出資
抗体医薬品事業に本格参入
http://www.fujifilm.co.jp/news_r/nrj1472.html
富士写真フイルム株式会社(社長:古森
重隆、以下「富士フイルム」)は、創薬系バイオベンチャーの株式会社ペルセウスプロテオミクス(社長:松田
和之、以下「ペルセウス」)による9億9,800万円の第三者割当増資を引受け、同社発行済株式の22.0%を有する筆頭株主となりました。富士フイルムは、今後、ペルセウスの持つガンや生活習慣病などの測定マーカーを用いた診断薬/システムの開発をはじめとして、抗体医薬品※1
事業を本格的に展開してまいります。
2006/3/13 東和薬品/沢井製薬/日医工
後発医薬品の規格取り揃えへの共同対応に関する基本合意のお知らせ
http://www.sawai.co.jp/press/2006/20060313.html
東和薬品株式会社(本社:大阪府門真市、社長:吉田 逸郎)、沢井製薬株式会社(本社:大阪市旭区、社長:澤井 弘行)及び日医工株式会社(本社:富山市、社長:田村 友一)は、後発医薬品の規格取り揃えに3社共同して包括的に対応することについて基本合意に至りましたので、下記のとおりお知らせいたします。
【本基本合意に至る経緯及び概要】
平成18年度薬価制度改革において、後発医薬品の普及促進が盛り込まれておりますが、その前提として、後発医薬品メーカーには、後発医薬品の必要な規格を揃えることが求められており、3月10日の厚生労働省医政局長通知により、その詳細が明らかになったところであります。それによりますと、「既収載後発医薬品であって、標準先発品が有する規格を有していないものについては、平成22年度末までに不足している規格の薬事承認を取得し、平成23年度末までに薬価基準収載の手続きを済ませ、安定供給を開始すること」等とされております。
後発医薬品メーカー各社は、本通知に従い後発医薬品の不足規格取り揃えに対応する必要がありますが、対応すべき規格数も多く、期間も限られていることから、その対応について3社で協議してまいりましたところ、今般、企業の枠を越え3社共同して包括的に対応することが最善との共通認識に至ったものです。
今後3社間での共同開発や薬事承認の小分けなどで各社不足規格の取り揃えを進め、真のジェネリック医薬品時代に向けた社会的要請に、迅速かつ的確に応えるべく邁進してまいります。
2006年4月6日 旭硝子
バイオ医薬品向け組換えタンパク質の製造設備の増設を決定
http://www.agc.co.jp/news/2006/0406.pdf
旭硝子株式会社(本社:東京、社長:門松正宏)は、バイオ医薬品原体の受託製造事業拡大のため、組換えタンパク質の製造設備の増設を決定しました。当社千葉工場(千葉県市原市)において、3000リットル規模の培養設備を含む新工場を建設することとし、本年10月に着工、2008年7月に商業生産を開始する予定です。
| <ご参考> |
| (1) |
発現系
:微生物や細胞に遺伝子を導入して培養し、タンパク質を作らせること。 |
| (2) |
cGMP:current Good
Manufacturing Practice
の略称。品質の良い優れた医薬品を製造するための要件をまとめた規準。WHOが1969年にGMPの採用を勧告して以来、医薬品製造に関する必須要件として世界各国において定着している。 |
| (3) |
ASPEX(アスペックス):Asahi
Glass Schizosaccharomyces pombe Expression System |
| (4) |
ASPEX事業の概要
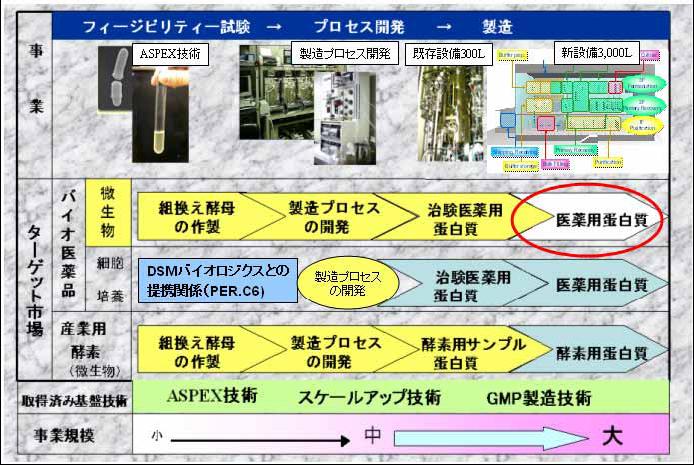 |
2006/6/1 旭化成メディカル/クラレメディカル
医療用中空糸膜製造合弁会社設立の件
http://www.asahi-kasei.co.jp/asahi/jp/news/2006/me060601.html
旭化成メディカル株式会社(本社:東京都千代田区
社長:吉田
安幸)とクラレメディカル株式会社(本社:東京都千代田区
社長:堀井
秀夫)は、(株)クラレが製造販売するEVOH樹脂(商標:エバール(R))を用いた医療用中空糸膜の製造会社を共同出資で設立することについて基本合意しましたのでお知らせいたします。
1.新会社概要
(1)会社名 : A・Kメンブレン製造株式会社
(英文名 A-K Membrane Manufacturing
Co., Ltd.)
(2)代表者 : 日吉
辰夫(旭化成メディカル(株)常務取締役)
(3)事業内容 : EVOH樹脂(商標:エバールR)を用いた医療用中空糸膜の製造及び供給
(4)設 立 : 2006年6月
(5)生産能力 :
400万本/年(スタート時260万本/年)
(6)所在地 : 宮崎県延岡市
(7)商業生産開始 : 2008年5月(予定)
(8)投資額 :
約25億円(初期投資約20億円)
(9)資本金 : 4億9千万円
(10)出資比率 :
旭化成メディカル(株)50%、クラレメディカル(株)50%
(11)従業員 : 約50名
2006/6/21 朝日新聞夕刊
薬害C型肝炎訴訟、国と製薬会社に賠償責任 大阪地裁判決
血液製剤「フィブリノゲン」などを投与されてC型肝炎ウイルス(HCV)に感染したとして、近畿、中国、四国地方の患者13人が国と製造元の三菱ウェルファーマ(旧ミドリ十字)、子会社のベネシスを相手に総額7億5900万円の損害賠償を求めた薬害C型肝炎集団訴訟の判決が21日、大阪地裁であった。中本敏嗣裁判長は原告13人のうち5人について国と製薬会社の責任を認め、4人は企業側の責任のみを認定し、総額2億5630万円の支払いを命じた。原告4人の請求は棄却した。
判決は「国は非加熱製剤の危険性が明らかになった87年4月以降も非加熱製剤の規制をせず、安全性を十分に確認しないまま加熱製剤を製造承認しており、安全確保に対する認識や配慮を著しく欠いており違法だ」と指摘した。
共同通信
汚染された血液製剤によるC型肝炎ウイルス(HCV)感染の被害を訴えた薬害肝炎訴訟で、大阪地裁が21日言い渡した判決は「規制権限を行使しなかったのは著しく不合理で違法」として国を批判、薬剤の安全性確保に厳格さを求めた。
中本敏嗣裁判長は原告13人のうち、国の違法性を認める分岐点とした1987年4月以降に血液製剤を投与された5人に対し、計約1億3600万円を製薬企業の三菱ウェルファーマ(旧ミドリ十字)と子会社の計2社と連帯して支払うよう国に命令。
企業への請求のみ認めた4人分と合わせた賠償総額は約2億5600万円で1人当たり約1300万-3600万円。投与時期で判断が分かれた。
旧ミドリ十字が昭和60年8月、ウイルスの感染力を奪う不活化処理の方法を変更して感染の危険性をいっそう高めた。
安全性確保義務に違反したとして、これ以降に製剤が投与された原告9人への損害賠償責任を認定
判決によると、旧ミドリ十字が85年8月にウイルスの不活化処理方法を変えた後のフィブリノゲンの感染カは「ほぼ100%近い確率」などと指摘。これ以降に投与された原告9人について、感染との因果関係を認め、製薬会社に賠償を命じた。中には、感染の可能性がある大量輸血を受けた人もいたが、「感染力の強いフィブリノゲンの投与が認められれば、輸血の有無にかかわらず、因果関係は推認される」と判断した。
国の違法性を認める分岐点とした1987年4月以降
国の責任について、旧厚生省の調査会が治療効果に疑問を抱く中、青森県での集団感染が発覚した87年4月時点で発生したと判断した。 国が製薬企業2社と連帯して支払う
国については、それ以前は、情報収集を怠るなどした国の対応を「医薬品の安全確保について意識が欠如していた」が
当時の状況に照らし、「著しく不合理とまでは言えない」と違法性は否定
日本経済新聞 2006/6/22
三菱ウェルに重いツケ
三菱ウェルファーマは三菱化学の製薬部門と旧ミドリ十字、旧吉富製薬、旧東京田辺製薬が2001年10月までに統合してできた。06年3月期の営業利益率は15%。新薬候補も多く収益基盤は底堅い。
ただ同社は賠償金の支払いに備えた会計上の引き当てをしていない。全国各地で係争中の訴訟では三菱ウェルヘの賠償請求は計55億円弱と賠償請求総額の96%を占める。今後の動向をにらみ、対応を検討する。
三菱ウェルファーマは旧ミリ十字製の血液製剤「フィブリノゲン」の投与で約1万人がC型肝炎を発症したと推計。潜在的な原告予備軍でもある被害者数は多く、今回の判決が新たな訴訟を促す公算は大きい。
ーーー
判決要旨
薬害C型肝炎訴訟で国と製薬会社に賠償を命じた21日の大阪地裁判決の要旨は次の通り。
【64年の非加熱フィブリノゲン製剤の製造承認について】
厚生大臣がフィブリノゲン製剤の製造承認をしたことが違法とはいえない。
旧ミドリ十字にも安全性確保に関する過失を認めることはできない。
【78年までの後天性低フィブリノゲン血症の適応除外について】
後天性低フィブリノゲン血症の適応除外をしなかった厚生大臣の規制権限不行使が著しく不合理であるとまではいえないから、いまだ違法とはいえない。
旧ミドリ十字にも安全性確保に関する過失はない。
【85年8月の不活化処理方法の変更】
C型肝炎(当時の非A非B型肝炎)の危険性や播種(はしゅ)性血管内凝固症候群(DIC)に関する知見がかなり集積されていた上、医療機器の進歩や医療技術の向上等により、産科領域においてフィブリノゲン製剤を必要とする症例は相当減少し、フィブリノゲンの有効性が疑問視される状況になりつつあった。
旧ミドリ十字は、85年8月、フィブリノゲン製剤の不活化処理方法について、約20年間にわたって行ってきた紫外線照射及びBPL併用処理から、ほとんど不活化効果がなかった紫外線照射等に変更したことにより、C型肝炎(当時の非A非B型肝炎)感染の危険性を一層高めたから、旧ミドリ十字には、安全性確保義務に違反した過失がある。
しかし、厚生大臣は旧ミドリ十字の不活化処理方法の変更を知っていたと認めるに足りる証拠はないから、その時点で、後天性低フィブリノゲン血症の適応除外をしなかった規制権限不行使が著しく不合理であるとはいえず、違法とはいえない。
【87年4月の非加熱フィブリノゲン製剤の規制権限不行使と加熱フィブリノゲン製剤の製造承認について】
肝炎の危険性やDICに関する知見がかなり明確になり、血液用剤再評価調査会が非加熱フィプリノゲン製剤の有効性、安全性、有用性に強い疑問を抱いていた中で、当時の医学的、薬学的知見に基づく有効性の審査方法の下では、フィブリノゲン製剤の有効性が確認できない状況にあった。当時、非加熱製剤について、青森県での肝炎集団発生事例の報告等があり、今後も同種感染事例の発生する危険性が高い状況にあった。
このような状況下にありながら、厚生大臣は、非加熱フィブリノゲン製剤について、後天性低フィブリノゲン血症の適応除外をしなかったから、規制権限不行使は著しく不合理であり違法である。
厚生大臣は乾燥加熱処理によってはウイルスの不活化は十分でなく、安全性が何ら確保されていないにもかかわらず、十分な調査、検討を行わず、当初から非加熱フィブリノゲン製剤に代えて加熱フィブリノゲン製剤の製造承認をするという結論ありきの方針の下に、申請からわずか10日で、有効性、安全性、有用性を実質的に十分に確認しないまま加熱フィブリノゲン製剤を製造承認した。厚生大臣の加熱製剤の製造承認は、安全性確保に関する認識や配慮に著しく欠けており、違法である。
旧ミドリ十字も、非加熱及び加熱フィブリノゲン製剤の製造、販売につき、安全性確保義務に違反した過失がある。
【原告9人の損害について】
フィブリノゲン製剤の違法な投与により、何らの落ち度がないにもかかわらず、C型肝炎ウイルスに感染し、その結果、深刻な被害を受けるに至ったものである。その損害は、C型肝炎の現在の病態と予後等から、無症候性キャリアの原告につき1200万円、慢性肝炎の原告につき3000万円を基礎損害額とし、病態の程度、これまでのインターフェロン治療歴、その他、原告ごとの個別事情を考慮して算定すると、各原告につき、1320万円から3630万円(弁護士費用を含む)、合計2億5630万円及び遅延損害金となる。
【請求棄却の原告4人について】
フィブリノゲン製剤の後天性低フィブリノゲン血症の適応除外に関し、その余の原告ら3人の旧ミドリ十字など2社と厚生大臣に対する損害賠償、請求を認めることはできない。
第9因子複合体製剤(クリスマシン)について、後天性血液凝固第9因子欠乏症の適応除外をせず、これを製造承認し、その後の規制権限を行使しなかった厚生大臣の行為に違法はない。
旧ミドリ十字の安全性確保に関する過失はない。
▽厚生労働省医薬食品局総務課医薬品副作用被害対策室の話
国の主張が一部認められず、厳しい判決。今後の対応は、関係省庁と協議し決定したい。厚労省としては引き続きC型肝炎対策の充実に努めていく。
▽三菱ウェルファーマの話
当社の主張が認められていない点もあり、今後の対応について慎重に検討したい。今後も医薬品の安全性の確保に最善の努力を尽くしていく。
読売新聞 6月23日
薬害肝炎訴訟、国が来週にも控訴
血液製剤「フィブリノゲン」によるC型肝炎ウイルス(HCV)感染について、国と製薬会社の責任を認めた薬害肝炎訴訟の大阪地裁判決を受け、厚生労働省は22日、来週にも判決を不服として大阪高裁に控訴する方針を固めた。
法務省と協議した上で、週明けに首相官邸に報告する。
大阪地裁判決について、厚労省内では「医薬品は、副作用と有効性のバランスを見て承認するかどうかを判断している。フィブリノゲンに大きな有効性があったのは明らか。このままこの判決を受け入れると、薬事行政が立ち行かなくなってしまう」という意見でほぼ一致している。
同日午後に行われた閣議後会見で、川崎厚労相は「(控訴について)時間をかけずに判断したい」と述べた。
日本経済新聞 2007/3/24
薬害C型肝炎 「国に責任」 東京地裁も 製薬3社の過失も認定
永野厚郎裁判長は「肝炎感染の危険性の警告を怠った」として国と製薬会社の責任を認定。13人に計約2億5900万円を支払うよう命じた。うち7人は製薬会社のみに賠償を命じた。
別の血液製剤「クリスマシン」などについては三菱ウェルファーマ(旧ミドリ十字)、日本製薬など製薬会社の責任を初めて認定。
同裁判長はフィブリノゲン投与による肝炎感染の過失責任が生じた時期について、国は加熱処理した同剤を製造承認した「87年4月以降」、製薬会社は社内で肝炎ウイルス処理法を変更した「85年8月以降」と認定。
毎日新聞 2007/8/1
薬害C型肝炎の救済拡大 名古屋地裁判決
製剤承認時から責任 国・企業に賠償命令
出産時などの止血のために投与された血液製剤でC型肝炎ウイルス(HCV)に感染したとして、患者が国と製薬会社3社を相手取り、総額約6億円の損害賠償を求めた薬害C型肝炎訴訟の判決が31日、名古屋地裁であった。松並重雄裁判長は「感染の危険性などを明確に表示する義務を怠った」として、国と会社に対し、原告9人のうち8人に総額1億3200万円の賠償を命じた。全国の同様訴訟で初めて、国と製薬会社に責任が生じる時期を製剤が承認された時点(76年)とし、投与時期で救済に差を設けなかった。
| 4地裁が認定した国と企業の責任 |
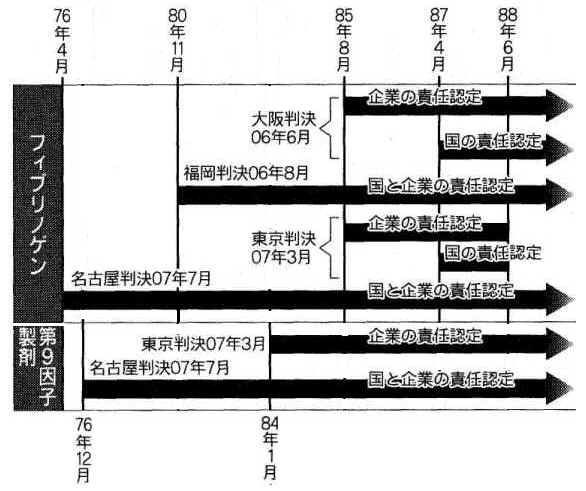 |
判決要旨
薬害肝炎名古屋訴訟で、国と製薬会社に賠償を命じた31日の名古屋地工裁判決の要旨は次の通り。
| 1 国及び三菱ウェルファーマ(WF)らのフィブリノゲン製剤に関する責任 |
| (1) |
適応限定義務違反
薬の「適応」を先天性低フィブリノゲン血症に限定せず後天性低フィブリノゲン血症も含めた点は、同製剤は後者にも有用性が認められるから、三菱WF、国などに過失や違法は認められない。 |
| |
|
| (2) |
指示・警告義務違反 |
| ア |
三菱WFらの責任 |
| |
同製剤は血清肝炎や非A非B型肝炎を発症する重大な副作用があり、慢性肝炎から肝硬変に移行し死に至る可能性もある。このため、同製剤の製造販売に当たっては、適応外の患者に広く使用されるのを防止し、安全を確保するために「血清肝炎ないし非A非B型肝炎ウイルス感染の危険を排除できないものであることを前提として、適応のある患者に限り治療上不可欠の場合に使用すべきである」(以下、注意内容と表記)旨を添付文書に明確な表現、表示方法をもって記載していなけれぱならなかった。
フィブリノゲンーミドリが76年に承認されて以降の添付文書には注意内容の記載が明確にされていると認めることができないから、三菱WFらは、低フィブリノゲン血症治療以外の目的で同製剤を投与された者に対して過失がある。 |
| |
|
| イ |
国の責任
厚生相(当時)は、同製剤の製造承認に当たり(三菱WFの前身である)ミドリ十字に、適応外の患者に対し広く使用されるのを防止し、安全を確保するために注意内容を添付文書に明確な表現、表示方法をもって記載させる措置を取らなければならなかった。しかし、厚生相は76年4月のフィブリノゲンーミドリ、87年4月のフィブリノゲンHTーミドリの製造承認に当たりこの措置を怠り、いずれの添付文書にも注意内容について、明確な記載がされなかったため賠償責任を負う。 |
| |
|
| 2 血液凝固第9因子複合体製剤(クリスマシンなど)に関する責任 |
| (1) |
適応限定義務違反
クリスマシンなどは後天性血液凝固第9因子欠乏症に対する有用性が認められるから過失を認めることはできない。 |
| (2) |
指示・警告義務違反 |
| ア |
三菱WFらの責任
クリスマシンにも同様の副作用がある。このため、製造販売の際適応外の患者に止血目的で便用されるのを防止し、また、後天性血液凝固第9因子欠乏症のうちビタミンK製剤などで治療することが可能な患者への投与を防止し、その投与を受ける患者の安全を確保するため、注意内容を添付文書に明確な表現、表示方法をもって記載しなけれぱならなかった。しかし、添付文書に記載が明確にされているとは認められず過失がある。 |
| |
|
| イ |
日本製薬の責任
PPSBーニチヤクにも同様の副作用があるため、76年末ころ以降、PPSB-ニチヤクを製造販売する際、注意内容を添付文書に明確な表現、表示方法で記載する義務があったが、添付文書には記載が明確にされていないから過失がある。 |
| |
|
| ウ |
国の責任
厚生相は76年12月、クリスマシンの製造承認に当たり、ミドリ十字に注意内容を添付文書に明確な表現、表示方法をもって記載させる措置を取らなければならなかったが、その義務を怠ったから、国家賠債法上の違法がある。PPSBーニチヤクについても同様の義務があったのに、添付文書に記載が明確にされなかった。さらにこれに代わる何らかの措置を取ったとは認められないから、権限の不行使は許容される限度を逸脱し著しく合理性を欠き、賠償責任を負う。 |
| |
|
| 3 付言 |
| |
ミドリ十字は85年8月の時点で、処理方法をウイルス不活化に十分な根拠のない手法に変え、感染の危険を増大させたのだから、危険が高まったことを記載すべき義務があったと言うべきである。ところが記載をしておらず、医薬品を便用する患者の安全を確保するという製薬会社の基本的義務に反したものであって、厳しい非難に値する。
ミドリ十字が安全確保をおろそかにする行動に出た背景には、厚生省の不適切な対応があったとみるべきで、医薬品を使用する患者の安全確保を図るという厚生行政の基本的責務に反したものとして、非難を免れることはできない。 |
2006/6/22 毎日新聞
■過去の主な薬害と被害者救済の経緯■
(カッコ内はおおよその被害時期と推定被害者数)
サリドマイド(1959~62年、約300人)
催眠剤 大日本製薬
74年、各地の集団訴訟の1審判決前に和解成立
スモン(55~70年、約1万1000人)
整腸剤キノホルム 日本チバガイキー(=武田製薬)、八洲化学(後に田辺製薬が吸収)と田辺製薬
78~79年に9地裁で原告勝訴判決が相次ぎ、和解成立
クロロキン(55~69年、約1000人)
抗マラリア薬 (長期投与によってクロロキン網膜症) 吉富製薬ほか関係製薬会社
88年、製薬会社の敗訴確定。95年の最高裁判決は国の責任を否定
ソリブジン(93年、15人死亡)
帯状疱疹(ほうしん)治療薬ソリブジン 日本商事
94年までに全遺族と製薬会社の示談が成立。国の責任は問われず
エイズ(83~85年、約2000人)
96年、東京、大阪訴訟の1審判決前に和解成立
クロイツフェルト・ヤコブ病(87~97年、約80人)
汚染されたヒト乾燥硬膜の移植 ビー・ブラウン・メルズンゲン・エージー、日本ビー・エス・エス
02年、東京、大津訴訟の1審判決前に和解成立
新3種混合(MMR)ワクチン(89~93年、約1000人)
03年に製造元の敗訴確定。今年4月の大阪高裁判決で国の責任認定
C型肝炎(64~88年、感染者は150万人以上)
06年6月21日、大阪地裁が国と製薬会社の責任を認める判決
ウィキペディア 薬害エイズ事件
薬害エイズ事件とは1970年代後半から1980年代にかけて、血友病患者に用いる血液製剤の原料である人血液・血漿を、主にHIV感染したと推定される外国の供血者から採り、非加熱処理でHIVに汚染された血液製剤を投与された患者がHIV感染し、それによる様々な病気で多数の死者を出した事件である。
日本ではドイツなどで加熱製剤が開発された後もなかなか承認されず、非加熱製剤を使い続けたためにエイズの被害が拡大したとされている。1989年5月に大阪で、10月に東京で後述の製薬会社と非加熱製剤を承認した厚生省に対して損害賠償を求める民事訴訟が提訴され、1996年2月に菅直人厚生大臣が謝罪し、3月に和解が成立した。
なお、このとき製造販売で提訴された製薬会社は、当時のミドリ十字と化学及血清療法研究所であり、輸入販売で提訴された製薬会社は、バクスタージャパン(日本トラベノール)と日本臓器製薬、カッタージャパンを合併承継したバイエル薬品(→バイエル社)である(カッタージャパンの該当非加熱製剤を発売元として大塚製薬と、同じくバクスター製の同種製品の輸入発売元として住友化学(現在の大日本住友製薬)の2社からも非加熱製剤を発売していた時期が有り、無関係では無かったが両社とも提訴されなかった)。
また、同年8月から10月に帝京大病院の医師だった安部英、厚生官僚だった松村明仁、製薬会社ミドリ十字(現在の三菱ウェルファーマ)の代表取締役だった松下廉蔵・須山忠和・川野武彦が業務上過失致死容疑で逮捕・起訴された。なお、安部の容疑は自らが担当した患者にHIVに汚染された非加熱製剤を投与して死亡させたことであり、HIVに汚染された非加熱製剤を流通させたことではない。
この裁判は2000年にミドリ十字の3被告人に実刑判決、2001年3月に安部に無罪判決、9月に松村に有罪判決が出た。2004年に認知症のために公判が停止されていた安部は2005年4月25日に死去した。
なお、安部に関しては、薬害エイズ事件の刑事責任を問うならば当時の関係者全員を問うべきで、いくら権威を持っていたとはいえ、安部だけに責任を負わせるのは酷であるとか、当時はHIVの危険性が不明で血友病の治療が優先されていたため、非加熱製剤の使用は仕方が無かったなどの意見もある。しかし被害者・世論の多くは、それで安部の責任が不問に付されるわけではないとして、無罪判決に批判的だった。
また、非加熱製剤によるHIV感染で刑事責任を追及した国は日本とフランスくらいで、安部のような臨床医の刑事責任を追及した国は日本だけである。
1996年8月にミドリ十字は株主代表訴訟を起こされ、2002年4月に和解した。
朝日新聞 2006/8/30
国と製薬会社に賠償命令 C型肝炎訴訟で福岡地裁判決
汚染された血液製剤を投与されC型肝炎ウイルス(HCV)に感染させられたとして、九州・沖縄などの患者18人が国と製造元の三菱ウェルファーマ(旧ミドリ十字)と子会社ベネシス(いずれも本社・大阪市)を相手取り、総額11億6600万円の損害賠償を求めた「薬害C型肝炎九州訴訟」の判決が30日、福岡地裁であった。須田啓之裁判長は原告18人のうち11人の訴えを認め、国と製薬会社に計1億6830万円の賠償を命じた。7人については請求を棄却した。
全国5地裁に提訴されたC型肝炎集団訴訟では6月の大阪地裁に続く司法判断だが、大阪と同様、原告が血液製剤を投与された時期・種類によって原告への賠償責任の有無が割れる形になった。
国の責任については(1)その時点の医学的知見の下で副作用を上回る有用性がある場合は製造承認は適法(2)副作用防止のため権限を行使しなかったことが著しく合理性を欠く場合は違法――との判断を示したクロロキン薬害訴訟最高裁判決(95年)が基準となった。
◆C型肝炎訴訟の主な争点◆
2006/8/31 毎日新聞
| |
原告側の主張 |
被告側(国・製薬会社)の主張 |
大阪地裁判決 |
福岡地裁判決 |
フィブリノゲンの
有効性、有用性 |
承認申請時のデータはずさんで大量出血の止血剤として効果はない |
多くの患者を出血死から救った医薬品。理論的にも有効性は明らか |
承認申請データはずさんだが、当時の知見から承認や再評価などの時点で有効性、有用性はあった
|
80年11月の時点では有効性が乏しく、危険性や代替製剤の存在からみて、有用性は認められなかった |
| 国と製薬会社の責任 |
感染の危険性や肝炎の重篤性を知りながら放置、被害を拡大させた |
当時の知見ではリスクを超えた安全性への疑念は生じていなかった |
国は青森で集団感染が起きた87年4月、企業はウイルス不活化処理方法を変えた85年8月以降に責任 |
80年11月以降のフィプリノゲンによる感染者について国と製薬会社に責任。クリスマシンは責任なし |
| 因果関係 |
製剤投与による感染率は高く、投与と感染の事実があれば証明十分 |
ウイルス不活化処理をしており、併用した輸血で感染した可能性も |
併用された輸血によってウイルス感染したとしか言えない事情があって初めて因果関係が否定される
|
原告番号2番は血液製剤を投与されていない可能性もあり被告に責任はない。母子感染の3番も同じ |
| 損害 |
最終的に肝がんに至る重篤な疾患で、症状ごとに定めた賠償を払え |
症状が進行しない患者もおり原告ごとに具体的損害額を示すべきだ |
基礎損害額を無症候性キャリアー1200万円、慢性肝炎3000万円とし、個別事情を加味して算定
|
C型肝炎の病態、治療状況、精神的苦痛などを考慮して1人当たり330万~2420万円の賠償が妥当 |
判決要旨
78年には米食品医薬品局(FDA)によるフィブリノゲン製剤の承認取り消しが公示され、当時の知見としてもフィブリノゲン製剤の有効性に疑問が生じていたのであるから、医薬品の安全性の確保等について第一次的な義務を有する旧ミドリ十字だけでなく、厚生大臣としても、その詳細を含めた情報を得た上で、非加熱フィブリノゲン製剤について調査、検討を行うべきであった。この時点で調査、検討を行えば、遅くとも80年11月までには、有効性及び有用性についての判断を行うことができたし、厚生大臣については、仮にそうでないとしても、旧ミドリ十字に対して緊急安全性情報を配布するよう行政指導すべきであった。
その結果、当時の知見によれば、非加熱フィブリノゲン製剤の有効性がないとされた蓋然性があるとまでは認められないものの、産科出血及びDICに対する知見が集積されるにつれ、その有効性が乏しいとされていた状況であって、そうした知見に加えてFDAによる承認取り消しによって示された知見や当時においては既に代替製剤が存在していたことなどからすると、この時点における判断として、非加熱フィブリノゲン製剤には後天性低フィブリノゲン血症に対する有用性が認められないとして、適応が制限された蓋然性が高い。
従って、旧ミドリ十字と厚生大臣は、遅くとも80年11月までに非加熱フィブリノゲン製剤の適応を先天性低フィブリノゲン血症に限定するか、または緊急安全性情報を配布すべき義務があったにもかかわらず、これを怠ったことに過失及び違法性がある。よって、被告会社らと国は、その後に同製剤の投与を受けた原告らに対する損害賠償義務を負う
(適応外使用の主張は理由がない)。
'
2006年7月21日 オリンパス
オリンパス、グローバルな免疫検査分野に本格参入
~生化学検査システムとの相乗効果で事業拡大を目指す~
http://www.olympus.co.jp/jp/news/2006b/nr060721immuj.cfm
オリンパス株式会社(社長:菊川 剛)は、2006年7月から免疫検査市場へ本格参入いたします。従来の生化学分析装置の技術・ノウハウを活かした免疫検査装置「AU3000i」と専用試薬を欧州から発売し、順次、米国、日本、アジアとグローバルに事業拡大をはかります。既存の生化学検査装置、および顧客サポート体制との相乗効果によって、当社の臨床診断検査事業全体の売上拡大をはかります。なお将来は、次世代医療のひとつに位置づける、遺伝子検査の臨床への応用を目指します。
「AU3000i」の概要
発売時期
欧州: 2006年7月(米国、日本その他の地域は未定)
| 主な特長 |
|
| 1)高い処理能力 |
|
24項目同時フルランダムアクセスにより、240テスト/hを実現
|
| 2)高い信頼性 |
|
サンプル詰まり検知の搭載による、データ信頼性の確保
自己診断機能の充実によるダウンタイムの削減
2次元バーコード採用による、試薬情報管理の充実
|
| 3)優れた操作性 |
|
生化学検査装置のAUシリーズと共通化して、変わらぬ操作性を実現
|
| |
|
|
| 基本仕様 |
| 測定項目 |
|
甲状腺ホルモン、性ホルモン、腫瘍マーカー
|
| 処理速度 |
|
240テスト/h |
| 同時分析可能項目 |
|
24項目 |
| 大きさ(mm) |
|
1700(W)×1190(D)×1435(H)
|
2006/8/9 ニプロ
エドワーズライフサイエンス社ブラジル法人の「人工心肺事業」買収に関するお知らせ
http://www.nipro.co.jp/topics/060809.pdf
ニプログループは、エドワーズライフサイエンス社のブラジル法人“Edwards
Lifesciences Comercio e Industria de Produtos Medico-Ciurgicos
Ltda”(以下「Edwards CPP」)における人工心肺事業の買収を行うことを決定しましたのでお知らせいたします。
1.買収の目的
当社は、昨年4月に大日本インキ化学工業株式会社(DIC)の人工肺事業の買収を行い、人工肺事業に本格的に参入しました。
人工肺にはその使用目的から、心臓の手術などで術中の体外循環に使用されるタイプと、心肺機能を補助する補助循環に使用される2つのタイプがあります。今回当社グループが買収を決定したEdwards
CPPの人工肺は前者のタイプであり、世界各国からニーズがあり現在約40カ国に供給されています。
Edwards CPPは人工肺の製造だけでなく、周辺の関連製品についても豊富に取り揃えています。
このように、当社グループは人工心肺関連製品のラインナップと販売チャンネルを承継することにより、世界的な人工心肺事業の展開をより一層強力に推進していきたいとの考えから、このたびの買収を行いました。
2.出資の内容
当社子会社のニプロメディカルLTDA(ブラジル現地法人)が100%出資し、Edwards
CPPの心肺事業に関する権利義務を承継し、Edwards
CPPは同社の完全子会社となります。薬事承認の状況によりますが、2006年中の取引完了見込みでございます。
3.エドワーズライフサイエンス社ブラジルの概要
(1) 会社名:Edwards Lifesciences Comercio e Industria de
Produtos Medico-Ciurgicos Ltda
(2)代表者: FERNANDO JORIO RODRIGUES
(3) 事業所所在地:2580 Avenida Santa Catarina in Sao Paulo
(4) 設立:1992年
(5) 主な事業内容:医療機器(特に人工心肺関連)の製造販売
Edwards Lifesciences
http://www.edwards.com/Japan/SharedPages/ourcompany.htm
|
カリフォルニア州アーバインに拠点を置くエドワーズライフサイエンス社は、重度の循環器疾患治療用製品の開発・製造・販売・サービスを手掛け、そのネットワークは世界100ヵ国以上。特に弁膜症治療に使用される人工心臓弁は世界のトップシェアを誇っています。
日本においても35年以上の実績を重ね、主に心臓血管、麻酔科、集中治療を専門に重篤な循環器疾患の治療用製品とサービスをご提供。先端の医療現場と連携し、より良い治療手段となる製品群の開発についても積極的に取り組んでいます。 |
本社所在地: Edwards
Lifesciences Headquarters One Edwards way, Irvine, CA. 92614
USA
代表者: マイケル・A.・ムサレム 会長兼最高経営責任者
従業員数: 約5,000人(全社総数)
各事業部本部: Irvine (弁膜症治療製品、クリティカルケア製品、血管治療製品、心臓外科製品)
Midvale (カニューレおよび心筋保護用製品)
製造施設: Irvine(カリフォルニア州)、Midvale(ユタ州)、
Sao
Paulo(ブラジル)、Haina(ドミニカ共和国)、Anasco(プエルトリコ)、
Horw(スイス)、宮崎(日本)
米国外拠点所在地: 東京、St. Prex(スイス)
2006/8/21 MerLion
Pharmaceuticals
MerLion Pharmaceuticals announces the completion of a merger with
Combinature Biopharm AG and Athelas SA and first closure of a
US$30M financing round
MerLion Pharma completes tripartite merger
Advanced antibiotic drug candidates moving into clinical trials
Significant Asian biotech financing round
Broad additions to technology platform for potential partnering
MerLion
Pharmaceuticals Pte Ltd (MerLion) of Singapore, the world’s leading natural products based
drug discovery company, announces that it has completed a merger
by exchange of shares with Combinature Biopharm AG (Berlin, Germany) and Athelas SA (Geneva, Switzerland). Both
European companies become 100% subsidiaries of MerLion whose
headquarters and drug discovery research centre is based in
Singapore. Drug development of its anti-infective programmes and
nuclear magnetic resonance screening activities will be conducted
from Berlin.
Note to Editors
About MerLion Pharmaceuticals http://www.merlionpharma.com/
MerLion Pharmaceuticals is the industry partner-of-choice in
natural products drug discovery. It maintains the world's largest
and most diverse collection of natural product samples and enters
multiple risk-share collaborations utilising its unique natural
products chemistry expertise and proven high throughput screening
capabilities.
The company’s current collaboration partners
include Abbott Laboratories, Arpida SA, Astellas Pharma Inc.,
Boehringer Ingelheim, Cancer Research Technologies Ltd, Dow
AgroSciences, the Institute of Molecular and Cell Biology
(Singapore), Johns-Hopkins (USA), Merck and Co, NovImmmune SA,
Nura Inc, Novartis Institute for Tropical Diseases, Sankyo Co
Ltd. and Schering-Plough Inc.
日本経済新聞 2006/8/29
医療機器 革新のうねり
患者に優しい新技術続々 光学・素材…強み生かす
薬の錠剤のように水と一緒にのみ込むだけで、内視鏡検査ができる。こんな技術が実用段階を迎えた。オリンパス子会社のカプセル型内視鏡は、SF映画「ミクロの決死圏」の潜航艇さながらに体内を巡り、がんなどを見つけ出す。
患者の肉体的な負担と経済的負担を両方軽減させるための工夫も加速している。日本の電機や素材の技術が原動力になっている。テルモが開発した新型のカテーテル(医療用細管)システムは、手足の血管から挿入して心臓まで達する手術が可能だ。長さ2メートル、太さは0.3ミリの細くて腰のある金属に独自の素材技術を盛り込んだ。
三菱電機は原子力発電所の技術を応用した高性能の「粒子線治療装置」事業で海外進出を狙う。エックス線を使う一般的な放射線治療装置より患部に集中させやすく、体の深部にある肺がんなどの治療に有効だ。一台40億円程度と高価だが、導入した病院には遠方から患者が押しかけ、海外からの引き合いも強い。
今年3月末、米大手のボストン・サイエンティフィックが同業の米ガイダントを買収、巨大医療機器メーカーが発足した。買収額は270億ドル(約3兆1200億円)にのぼった。独シーメンスも6月末、バイエルの診断薬事業を買収。有力技術を狙うM&Aの流れは止まらない。
国内審査、長い道のり 厳しい基準、産学官で克服
欧米の2世代前
手術ロボに助成
産学官の医療機器の専門家らで構成するコンソーシアムは今春、遺伝子診断機器や除細動器など7テーマを選び、国や産業界が協力すれば日本の強みを生かせる医療機器開発が可能との提言をまとめた。企業は医療現場と対話をしながら、挑戦していく必要がある。
2005/1/25 ライブドア・ニュース
米ボストン・サイエンティフィック
Boston Scientific、3.1兆円でガイダントGuidant
を買収へ=J&Jとの買収合戦に勝利
AP通信によると、米医療機器大手ガイダントは25日、同業の米ボストン・サイエンティフィックに約272億ドル(約3兆1000億円)で身売りすることで合意した。米日用品大手ジョンソン・エンド・ジョンソン(J&J)との間で繰り広げられていた買収合戦は、ボストン・サイエンティフィックの勝利に終わった。
2006/1/12 http://management.blog45.fc2.com/blog-entry-116.html



